Что такое ips клетки
Со времени, когда профессору Киотского университета Яманаке Синъя удалось создать iPS-клетки человека (искусственные плюрипотентные стволовые клетки), прошло 10 лет. Сейчас, когда уже начались испытания созданных с использованием этих клеток лекарственных препаратов для борьбы с трудноизлечимыми заболеваниями, прикладные исследования, ведущие к лечебной практике, уверенно продвигаются вперёд.
- English
- 日本語
- 简体字
- 繁體字
- Français
- Español
- العربية
- Русский
Что же делать?
Решать вышеперечисленные проблемы можно с помощью двух независимых стратегий. Первая стратегия заключается в поиске альтернативных безопасных способов введения транскрипционных факторов*. На сегодняшний день в этом направлении ведется множество работ. Например, в качестве поставщика генов ТФ используют аденовирусные конструкции, не встраивающиеся в клеточный геном. При другом подходе ТФ доставляют в клетку не в виде генов, а в виде РНК-матриц или готовых белков. Даже в рамках интегративных методов доставки транскрипционных факторов ведутся работы по снижению рисков их использования за счет встраивания всех четырех генов в одну рамку считывания. Вариантов доставки факторов транскрипции в клетку очень много, но все они проигрывают привычным лентивирусным конструкциям по двум параметрам — по эффективности и оптимальности материальных затрат и сил. Последнее тоже немаловажно, так как в перспективе перепрограммирование клеток будут производить не в лабораторных, а в медицинских масштабах.
* — Редкий человек не слышал о дурном поведении чужих и даже собственных по каким-то причинам слабо контролируемых стволовых клеток: «Ствол и ветки, стволовые клетки» [1]. Методология получения ИПСК ещё больше повышает градус онкологической настороженности: проблему представляет встраивание в геном не только векторной ДНК с активными промоторами, но и протоонкогенов — да, гены двух из четырех «магических» ТФ (c-Myc и Klf4) относятся к протоонкогенам. Поэтому стараются всеми способами найти баланс между эффективностью перепрограммирования и безопасностью, меняя спектр ТФ или вовсе исключая введение генно-инженерных конструкций — есть надежда, что в перспективе будет достаточно просто «похимичить»: «Снежный ком проблем с плюрипотентностью» [10], «Была клетка простая, стала стволовая» [9]. — Ред.
Вторая стратегия заключается в поиске оптимального типа клеток для перепрограммирования. Оказалось, что разные типы клеток могут значительно различаться по своей способности давать линии ИПСК. Эти различия проявляются в неодинаковых скорости и эффективности (из одного и того же количества клеток разных типов получается разное количество клонов ИПСК) перепрограммирования. Способность клеточного типа к перепрограммированию зависит от разных факторов. Некоторые клетки являются мультипотентными или просто активно обновляющимися, что ставит их ближе, чем терминально дифференцированные клетки, к плюрипотентному состоянию.
Кроме эффективности такого превращения, клетки отличаются числом транскрипционных факторов, необходимых для их перепрограммирования. Клетки, «откликающиеся» на меньшее число факторов транскрипции, не только значительно сокращают риски даже опасных способов введения ТФ, но и увеличивают эффективность уже найденных безопасных. К таким клеткам относятся, к примеру, нейроны, способные перепрограммироваться при введении не четырех, а всего лишь одного транскрипционного фактора [13]. Но нейроны не подходят для повсеместного создания ИПСК в медицине из-за сложности их выделения из организма. Помимо простоты получения оптимальный тип клеток должен быть в наименьшей степени подвержен агрессивному воздействию внешней среды, а значит, к таким клеткам нельзя отнести кожные фибробласты, наиболее часто используемые для перепрограммирования [14].
Выход на этап клинических исследований в регенеративной медицине: глазная сетчатка, сердечная мышечная ткань и др.
В регенеративной медицине, которая является ещё одним важным направлением клинического использования iPS-клеток, в 2013 году Институт физико-химических исследований RIKEN в рамках проекта под руководством Такахаси Масаё приступил к клиническим исследованиям метода лечения трудноизлечимой возрастной макулодистрофии, использующего клетки, полученные из iPS-клеток. Вслед за этим в Осакском университете профессор Сава Ёсики (генеральный директор Японского научного общества регенеративной медицины) в ближайшем будущем намеревается приступить к клиническим опытам по пересадке пациентам с тяжёлыми заболеваниями сердца сердечных мышечных тканей, изготовленных из iPS-клеток. Эта разработка была проведена совместно с корпорацией Terumo.
Уже упомянутый профессор Окано Хидэюки из Университета Кэйо также ведёт подготовку к пересадке пациентам с повреждениями спинного мозга нейрональных стволовых клеток, полученных путём преобразования iPS-клеток. Кроме того, профессор Такахаси Дзюн из центра исследований iPS-клеток Киотского университета в августе 2017 года объявил о том, что в результате пересадки обезьяне с симптомами болезни Паркинсона нервных клеток, полученных из iPS-клеток, произошло ослабление дрожания верхних и нижних конечностей, а также других симптомов. Впервые подтвердив эффект на близких к человеку приматах, исследователи ставят целью приступить к клиническим опытам уже в 2018 финансовом году.
В более отдалённой перспективе исследователи мечтают создавать целиком отдельные жизненно важные органы. Профессор Сава Ёсики, говоря о регенеративной медицине через 30 лет, отметил: «Если речь идёт о таких органах с простыми функциями, как, к примеру, сердце, чья работа состоит в сжатии – возможно, мы сможем создавать такие органы целиком».
В Центре исследований iPS-клеток, который возглавляет профессор Яманака Синъя, в 2013 году начали работу по созданию банка iPS-клеток из материала людей, чей тип иммунитета отличает слабость реакции отторжения, и уже в 2017 году этот банк будет состоять из iPS-клеток типов, подходящих для 30 процентов японцев. Банк будет поставлять эти iPS-клетки и для клинических опытов по лечению возрастной макулодистрофии, а также по пересадке сердечных мышечных тканей. Вместе с тем на пути к клиническому использованию, опираясь на фундаментальные исследования iPS-клеток, предстоит решить целый ряд задач, главные из которых – предотвращение преобразования в раковые клетки, повышение качества клеточного материала и преобразование в клетки различных органов.
Фотография к заголовку: профессор Осакского университета Сава Ёсики на пресс-конференции после подачи заявки на проведение клинических исследований лечения сердечной недостаточности с использованием iPS-клеток, 21 июля 2017 г., преф. Осака, город Суйта (фотография предоставлена Jiji Press)
В августе исполнилось 10 лет со времени публикации научной статьи профессора Киотского университета Яманака Синъя, в которой сообщалось о создании iPS-клеток (искусственном создании плюрипотентных стволовых клеток). В 2014 году были проведены клинические исследования по трансплантации пациенту тканей клетчатки, произведённых из iPS-клеток. Надежды людей сталкиваются с задачами, требующими решения. Тем не менее, продолжается уверенное продвижение к созданию новых методов лечения.
- English
- 日本語
- 简体字
- 繁體字
- Français
- Español
- العربية
- Русский
Идея регенеративной медицины одновременно стара и нова. Человек издавна мечтал о возможности вернуть утраченное зрение, силу обездвиженным конечностям, заставить биться с новой силой изношенное сердце. В широком смысле к регенеративной медицине можно отнести очки и протезы, искусственные органы и другие заменяющие средства. Метод клеточной терапии, преследовавший цель решить все эти задачи путём пересадки клеток, привлёк к себе живое внимание 35 лет назад. В 1981 году были получены эмбриональные стволовые клетки (ES-клетки) из эмбриона мышей, а в 1998 году – ES-клетки человека.
Около 60 триллионов клеток взрослого организма человека образуются благодаря многократному делению, началом которого служит одна-единственная оплодотворённая яйцеклетка. Стволовые клетки при делении способны не только воспроизводить сами себя, но и преобразовываться в различные другие типы клеток (то есть обладают плюрипотентностью). Таким образом из оплодотворённой яйцеклетки производятся самые различные клетки, составляющие живой организм.
Эмбриональные стволовые клетки получают из эмбриона ранней стадии – всего после 6-7-кратного деления оплодотворённой яйцеклетки. Эти обладающие свойством плюрипотентности (способностью преобразовываться в разнообразные клетки, формирующие живой организм) клетки можно размножать практически без ограничений. С одной стороны, на ES-клетки возлагают большие надежды как на исходный клеточный материал для регенеративной медицины. В то же время на этом пути остаётся ряд нерешённых задач. Это и технология безопасного стимулирования преобразования в необходимый вид клеток, и технология подавления реакции отторжения, и, наконец, самое серьёзное препятствие: морально-этическая проблема, связанная с тем, что материал производится из оплодотворённых человеческих яйцеклеток.
В обстановке, когда весь мир занимался исследованиями, стремясь заставить эмбриональные стволовые клетки преобразовываться нужным образом в ткани организма, профессор Яманака пошёл совершенно иным путём, который и привёл его к успеху в получении плюрипотентных стволовых клеток, не уступающих эмбриональным стволовым.
Клетки дермальной папиллы — возможный ключ к решению проблем

Рисунок 1. Строение волосяного фолликула. Дермальная папилла, или волосяной сосочек, находится в основании волосяной луковицы.
В 2011 году было показано, что клетки дермальной папиллы мыши также можно перепрограммировать с помощью всего лишь одного ТФ — Oct4 [15]. С тех пор идея перепрограммирования клеток дермальной папиллы больше не выдвигалась, что кажется весьма странным, поскольку эти клетки как нельзя лучше подходят на роль источника ИПСК. Дермальная папилла (ДП) — это соединительнотканный сосочек в волосяной луковице (рис. 1); он находится в глубоких слоях кожи и в меньшей мере подвержен агрессивным воздействиям окружающей среды. Кроме этого, клетки ДП удобны для выделения: для получения культуры клеток достаточно нескольких выдернутых волос. Но что самое главное, эти клетки легко поддаются перепрограммированию и требуют меньше вмешательств в транскриптом, что значительно безопаснее по сравнению с классическим перепрограммированием четырьмя транскрипционными факторами. К сожалению, работа проводилась на мышиных клетках [15], а на человеческих ее результаты проверены не были.

Рисунок 2. Результат от-ПЦР-анализа клеток дермальной папиллы человека, терминально дифференцированных фибробластов и ИПСК на экспрессию факторов Яманаки. Можно видеть, что в клетках дермальной папиллы присутствуют три из четырех транскрипционных факторов. Рисунок из диплома автора статьи [16].
Как следствие, в 2014 году в лаборатории генетики развития Института общей генетики им. Н. И. Вавилова в рамках одной из дипломных работ была поставлена следующая задача: определить минимальный набор транскрипционных факторов, необходимых для перепрограммирования клеток дермальной папиллы. Для начала было проведено более детальное изучение экспрессии генов транскрипционных факторов в клетках дермальной папиллы человека. Оказалось, что в этом типе клеток в обычном состоянии экспрессируются гены трех из четырех ТФ Яманаки: SOX2, KLF4 и c-MYC (рис. 2). Факт экспрессии KLF4 и c-MYC не удивляет, так как их продукты участвуют в процессах пролиферации и регуляции клеточного цикла и присутствуют в дифференцированных клетках — например, в кожных фибробластах. Но Sox2 является фактором плюрипотентности и встречается в уже перепрограммированных ИПСК, где есть все ТФ; в этом клетки дермальной папиллы уникальны. Таким образом, если в этих клетках уже синтезируются три из четырех транскрипционных факторов, действительно есть основания полагать, что перепрограммирование клеток ДП человека с помощью одного лишь фактора Oct4 осуществимо.
При дальнейших исследованиях выяснилось, что клетки ДП человека хуже поддаются перепрограммированию, чем аналогичные клетки мыши — оно идет значительно дольше и с меньшей эффективностью. Это вполне логично, так как волосяной покров человека в процессе эволюции изменил свои физиологические функции по сравнению с покровом остальных млекопитающих. На данный момент удалось провести перепрограммирование только с помощью двух ТФ — Oct4 и Sox2 (рис. 3), — что уже является неплохим результатом, так как сокращает вдвое вышеописанные риски повреждения генома при использовании вирусных конструкций [16].
Встает закономерный вопрос: почему для перепрограммирования потребовалось более одного транскрипционного фактора, если в клетках и так присутствуют три из них? Видимо, естественной экспрессии генов ТФ в клетках дермальной папиллы оказалось недостаточно для перестройки генома в плюрипотентное состояние, и для перепрограммирования одним фактором транскрипции понадобятся вспомогательные низкомолекулярные агенты, облегчающие его работу. По некоторым данным, малые органические молекулы даже без прямого влияния на активность генов способны «катализировать» переведение клеток в плюрипотентное состояние, заменяя при этом часть ТФ [9].

Рисунок 3. ИПСК, полученные из клеток дермальной папиллы человека. А — Характерная морфология плюрипотентных стволовых клеток: плотные колонии из мелких клеток с высоким ядерно-цитоплазматическим соотношением. Б — Окраска ИПСК на маркеры плюрипотентности Oct4, Nanog, Tra 1-60 и SSEA4, наличие которых доказывает завершение перепрограммирования. Рисунок из диплома автора статьи [16].
Конечно, за один год дипломной работы пропасть между теорией и практикой автором этой статьи преодолена не была, однако дальнейшие пути исследований вырисовываются четче. Приведенные выше результаты показали, что клетки дермальной папиллы действительно находятся ближе к плюрипотентности, чем обычные терминально дифференцированные клетки, и исследования перепрограммирования клеток ДП человека одним транскрипционным фактором нужно продолжать. Вероятно, в ближайшее время в других лабораториях, где занимаются альтернативными безопасными способами введения факторов транскрипции, тоже найдется оптимальное решение, и, сложив два и два, мы таки придем к медицине будущего.
Перспективы использования стволовых клеток в медицине
С момента появления технология получения ИПСК была существенно усовершенствована. В частности, теперь не нужно использовать векторы на основе ретровирусов, которые встраиваются в произвольное место генома и могут повредить его или даже запустить программу онкологической трансформации. Теперь используют аденовирусы или другие вирусные векторы, не встраивающиеся в хромосомы, а также РНК, белковые транскрипционные факторы и эписомальные плазмиды. В некоторых случаях число перепрограммирующих факторов можно снизить до одного — например, нейрональные стволовые клетки мыши превращаются в ИПСК введением одного только фактора Oct4 [12].
Открытие Яманаки также сообщило новый импульс поиску способов трансдифференцировки — то есть, превращению одного типа клеток в другой, минуя стадию стволовых клеток. Это возвращает нас в 1960–80-е годы, к работам по имагинальному диску дрозофилы и к таким генам как Antennapedia, MyoD, GATA1 и Pax5. В частности, уже тогда удалось превратить фибробласты в миобласты активацией гена MyoD [13]. Под впечатлением от работ Яманаки быстро нашли способ превратить экзокринные клетки поджелудочной железы в эндокринные [14], а фибробласты — в кардиомиоциты [15]. Есть даже пример превращения друг в друга клеток разных зародышевых листков — мезодермальных фибробластов в эктодермальные нейроны (на что потребовалось три транскрипционных фактора) [16].
Наиболее трепетные ожидания, связанные со стволовыми клетками, заключаются в возможности замещать больные или утраченные клетки прямо в ткани, восстанавливая организм буквально по клеточкам. В самом общем виде такая формула подходит для лечения практически любой болезни — хоть Альцгеймера, хоть Паркинсона, хоть диабета, хоть последствий инфаркта. Конечно, это все находится в туманной дымке светлого будущего, но некоторые реальные перспективы тоже есть. В частности, клеточная терапия с применением ИПСК обещает освободить врачей от проблемы иммунной несовместимости. Конечно, особое внимание нужно уделить безопасности — ведь, как уже было сказано, ИПСК могут иметь как привнесенные при перепрограммировании мутации, так и быть онкогенными сами по себе. В общем, несмотря на то, что ИПСК сулят совершенно баснословные преимущества для медицины, пока что имеется «снежный ком» проблем, связанных с ними [17].
Другая перспектива, уже ставшая твердой действительностью, — возможность получать линии бессмертных клеток (ИПСК), соответствующих различным редким генетическим заболеваниям, и изучать как саму болезнь, так и действие на нее разрабатываемых лекарственных средств (рис. 4) [18]. ИПСК уже получены для таких заболеваний как амиотрофический латеральный склероз (болезнь Шарко), синдром Ретта, спинальная мышечная атрофия (СМА), недостаточность антитрипсина α1, семейная гиперхолестеринемия, а также для различных кардиологических заболеваний. В некоторых из этих клеточных моделей удается связать наблюдаемый фенотип с болезнью: в частности, в случае клеток из СМА, это затухание функций моторных нейронов. Некоторый прогресс есть даже в изучении заболеваний со сложной генетикой, таких как шизофрения.

Рисунок 4. ИПСК в медицине. Из тканей пациентов, страдающих различными заболеваниями, можно выделить соответствующие клетки и превратить их в ИПСК. Колонии этих клеток можно дифференцировать в другие типы клеток и использовать их в лечении, или же изучать на них болезнь и действие лекарств.
Исследуют на культурах специфичных для конкретных болезней ИПСК и действие разрабатываемых лекарств. В частности, на модели наследственной вегетативной дистонии проведен скрининг базы химических веществ и найден прототип лекарства кинетин, который способен частично обратить последствия нарушенного сплайсинга гена IKBKAP, вызывающего эту болезнь [19]. Аналогично, показано лекарственное действие бета-блокаторов и блокаторов ионных каналов на ИПСК из модели синдрома удлинения QT интервала [20]. Так ИПСК уже вошли если не в клиническую, то в лабораторную практику и служат «испытательными стендами» для изучения различных болезней и действия на них разрабатываемых лекарств.
Открытие того, что зрелые дифференцированные клетки можно вернуть в плюрипотентное состояние или даже, минуя его, превратить один тип клеток в другой, стало поворотным в эмбриологии, биологии развития и всей молекулярной биологии. Это знание уже осветило все уголки физиологии и медицины, и практические применения в виде новых видов лечения наверняка не заставят себя ждать.

Обзор
Автор
Редактор
Статья на конкурс «био/мол/текст»: Открытие индуцированных плюрипотентных стволовых клеток (ИПСК) стало одним из самых громких и многообещающих достижений в научном мире за последние годы. Казалось бы, как только у каждого человека появятся свои собственные плюрипотентные стволовые клетки, разрешится огромное количество медицинских проблем. Тем не менее прошло уже почти десять лет, а применение ИПСК в реальной практической медицине толком еще и не начиналось. По-прежнему между открытием ИПСК и спасением мира от всех недугов стоит основная проблема — методы индукции плюрипотентности в клетках. Способом преодолеть эту пропасть может быть поиск клеточных типов, легче поддающихся перепрограммированию. Один из этих типов лежит буквально «на поверхности» — клетки дермальной папиллы.
Обратите внимание!
Эта статья опубликована в номинации «Своя работа» конкурса «био/мол/текст»-2015.
Спонсором номинации «Лучшая статья о механизмах старения и долголетия» является фонд «Наука за продление жизни». Спонсором приза зрительских симпатий выступила фирма Helicon.
Спонсоры конкурса: Лаборатория биотехнологических исследований 3D Bioprinting Solutions и Студия научной графики, анимации и моделирования Visual Science.
Какие могут быть проблемы?
Несмотря на активное изучение ИПСК, существует ряд проблем, затрудняющих их использование непосредственно для лечения человека. Эти проблемы связаны со способом индукции плюрипотентности («перепрограммированием») клеток. Надо сказать, еще совсем недавно даже мысль о существовании таких способов относилась к категории еретических, ведь дифференцировка считалась процессом необратимым — до «нобелевских» работ Джона Гёрдона и Синьи Яманаки [8]. Как установила группа Яманаки, для перепрограммирования терминально дифференцированных клеток необходимо всего четыре транскрипционных фактора: Oct4, Sox2, c-Myc и Klf4 [9]. Транскрипционные факторы (ТФ) — это белки, способные регулировать работу генов. При работе этих четырех ТФ геном клетки перестраивается в плюрипотентное состояние. На данный момент единственным эффективным способом получения ИПСК является внесение генов ТФ в клетку с помощью лентивирусных векторных конструкций. Такой метод приводит к интеграции вектора в геном клетки, что может вызвать непредвиденные модификации его структуры и привести к развитию злокачественных образований. Кроме этого, сами вирусные конструкции являются антигенами для человека, что также небезопасно и ограничивает возможности практического применения ИПСК [10].
Атака клонов
Работы Гардона положили начало технологии, называемой терапевтическим клонированием (somatic cell nuclear transfer). В 1997 году с помощью этого метода (конечно, с существенными изменениями) появилась на свет знаменитая овечка Долли [5]. Важным дополнением стало то, что ядро перед пересадкой ввергали в покоящееся состояние, что позволяло лучше «синхронизовать» ядро с клеткой, его лишенной. С тех пор уже удалось клонировать довольно много млекопитающих — не только овцу, но и мышь, корову, свинью, волка и степного кота. Метод пересадки ядер также позволил совершить ряд важных открытий в иммунологии.
Перепрограммирование с помощью ядра соматической клетки
Первые попытки пересадки ядер были сделаны не Гардоном; еще в 1952 году Бриггс (Robert Briggs) и Кинг (Thomas King) разработали технологию «пересадки» ядра соматической клетки лягушки Rana pipiens в оплодотворенную икринку, ядро которой предварительно разрушали [2]. Амфибии хорошо подходят для таких экспериментов, потому что их икра крупная и развивается не внутриутробно. В этой работе было показано, что пересадка ядра из эмбриональных клеток действительно может дать начало нормальному головастику, но аналогичный опыт с более дифференцированными клетками к успеху не привел. Поэтому, хотя фактически они проделали ту же работу, что и Гардон несколькими годами позже, им пришлось сделать вывод, что дифференцированные клетки необратимы в своем развитии [3].
Джон Гардон, эмбриолог, закончивший Оксфорд, выбрал для своих опытов другую лягушку — «ветерана» лабораторных исследований Xenopus laevis. Он уничтожал ядро яйцеклетки ультрафиолетовым светом и пересаживал в цитоплазму ядро от дифференцированной клетки эпителия, и в части опытов ему удалось получить нормально плавающих и развивающихся головастиков (рис. 2; [4]). Так что Гардону, в противоположность своим предшественникам, удалось показать именно то, что пересадка ядра от дифференцированных клеток способна вернуть генетическую программу к состоянию плюрипотентности. Однако много лет прошло, прежде чем научное сообщество восприняло эти революционные работы всерьез.

Рисунок 2. Перепрограммирование ядра клетки эпителия лягушки. Гардон использовал ультрафиолет, чтобы разрушить ядро икринки лягушки (1), а потом пересаживал туда другое ядро, полученное из эпителия головастика (2). В большинстве случаев клетки погибли, однако несколько из них развились в головастиков и затем — во взрослых лягушек (3). Этот опыт подтвердил, что генетическая информация сохраняется неизменной на протяжении всего срока жизни клетки, и может в подходящих условиях быть задействована вновь. Более поздние исследования, основанные на том же принципе, привели к клонированию млекопитающих (4).
Исследования Гардона подвели подкоп под парадигму необратимости развития, впервые наглядно продемонстрировав, что ядро дифференцированной клетки вполне может быть возвращено на плюрипотентный этап и дать начало всем типам соматических и половых клеток, — если его поместить в цитоплазму яйцеклетки, «настроенной» на этот режим.
Создание юридической базы поможет скорейшей реализации мечты о регенеративной медицине
На пути к практической реализации методов лечения с использованием iPS-клеток государство оказывает поддержку, занимаясь решением задач юридического и прочего характера. В ноябре 2014 года были внесены поправки в прежний Закон о фармацевтике. В отношении клеточных тканей и других «изделий регенеративной медицины» государство подтвердило: в случае, если безопасность проверена, государство разрешает использовать такой материал в качестве медицинского препарата на этапе, когда он считается эффективным, в ограниченные сроки и для ограниченного круга покупателей. Что касается эффективности, то в случае, если по истечении определённого срока продажи она поддаётся проверке, материал получает официальное утверждение после прохождения соответствующих обследований. Если по старому закону для получения разрешения требовалось более десяти лет, то теперь можно ожидать сокращения этого срока до 2-3 лет.
Хотя новое законодательство рассматривают как наиболее передовое на мировом уровне, в то же время можно утверждать, что оно является проявлением решимости идти на определённый риск, поскольку Япония признаёт средства регенеративной медицины прежде, чем остальной мир.
С другой стороны, новый закон принят и в целях защиты пациентов – чтобы предотвратить «серое» (не попадающее под действие системы медицинского страхования) применение на свой страх и риск методов регенеративной медицины, безопасность и эффективность которых ещё не определена.
Предыстория
В процессе нормального развития каждая клетка проходит путь от изначального недифференцированного состояния, характерного для оплодотворенной яйцеклетки (зиготы) и клеток раннего эмбриона, до специализированных клеточных форм, медленно делящихся и служащих для выполнения всего спектра клеточных функций (рис. 1а). Наиболее «многофункциональную» клетку — зиготу — называют тотипотентной, то есть, дающей начало абсолютно всем другим типам клеток.
По мере развития, клетки становятся все более специализированными и все менее подверженными «неожиданным» превращениям. Во взрослом организме число стволовых клеток невелико, и они располагаются в строго определенных местах (например, костном мозге), играя роль источника для пополнения популяции дифференцированных клеток. Эта закономерность и сформировала представление, что развитие клеток возможно лишь в одном направлении, и никогда дифференциация не обернется вспять. Конрад Уэддингтон (Conrad Hal Waddington) использовал метафору горного ландшафта, в которой плюрипотентная клетка находится на вершине горы, а специализированные клетки лежат в долинах, «скатываясь» каждая по своей траектории (изображающей путь дифференциации) (рис. 1б). Эта метафора подчеркивает сложность или невозможность обратного пути «в гору» и, значит, превращения одних клеток в другие.

Рисунок 1. Развитие организма и дифференциация клетки. а — Нормальное развитие человека из оплодотворенной яйцеклетки до взрослого организма иллюстрирует идею однонаправленного процесса развития. б — Иллюстрация Уэддингтона [1] для процесса клеточной дифференциации. «Эпигенетический ландшафт» задает путь, который проходит каждая клетка в процессе обретения специализации. Эти картина призвана подчеркнуть, что путь «обратно» невозможен или сильно затруднен.
Однако теоретическая возможность «перепрограммирования» не исключалась полностью; Ханс Шпеман, нобелевский лауреат по физиологии и медицине 1935 года, первым предложил идею «пересадки» ядер дифференцированных клеток в цитоплазму яйцеклетки, чтобы изучить способность к дифференциации.
Стволовые клетки, не вызывающие сомнений в этичности: Нобелевская премия 2012 года
Из 24-х генов, часто выявляемых в эмбриональных стволовых клетках, были определены четыре, которые впоследствии стали называть «генами Яманаки» (Oct3/4、Sox2、Klf4、c-Myc). При внедрении этих генов в кожные клетки мышей с использованием ретровируса в качестве доставщика генетического кода (вектора) были получены плюрипотентные стволовые клетки, подобные эмбриональным стволовым. В названии клеток – iPS-клетки (induced pluripotent stem cell, «индуцированная плюрипотентная стволовая клетка») – была намеренно использована маленькая буква i по аналогии с получившим тогда распространение по всему миру продуктом фирмы Apple – компактным аудиоплеером iPod.
Детальная техника получения, а также состав четырёх генов были опубликованы в британском научном журнале Cell от 25 августа. Но для того, чтобы использовать iPS-клетки при лечении человека, требовалось получить их из человеческого материала. В случае эмбриональных стволовых клеток для перехода от мышиного материала к человеческому потребовалось 17 лет. В создании iPS-клеток человека профессор Яманака добился успеха уже в 2007 году.
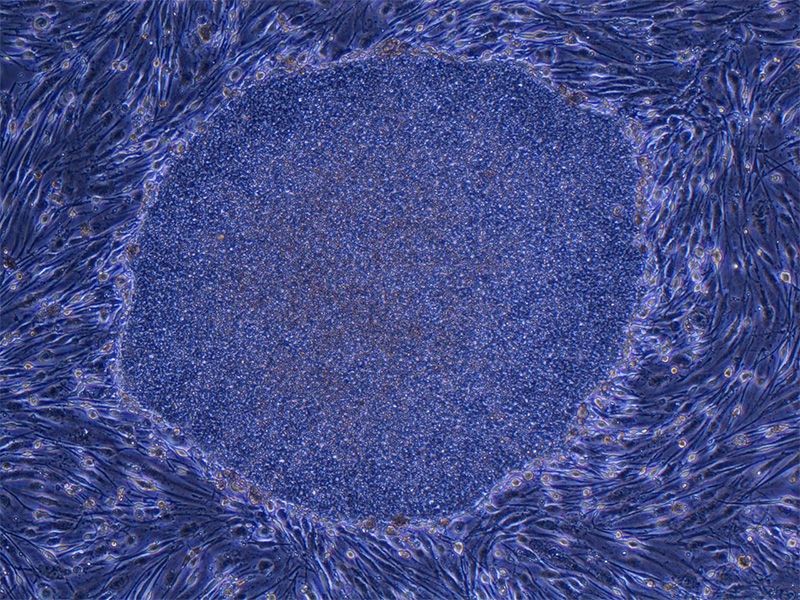
Колония (группа) iPS-клеток человека, выращенных из клеток фибробласта (соединительной ткани). Размер колонии – приблизительно 0,5 мм в поперечнике (фотография предоставлена профессором Яманака Синъя)

Профессор Яманака Синъя отвечает на вопросы на форуме для учащихся полных средних школ, который состоялся 4 ноября 2011 года в Токио (фотография предоставлена Центром исследований iPS-клеток Киотского университета)
В iPS-клетках скрыт потенциал, который способен изменить всю клиническую медицину в целом, не ограничиваясь регенеративной медициной. К примеру, они породили надежду на то, что сопоставление инициализированных iPS-клеток человека с клетками его поражённых заболеванием органов позволит понять механизм развития заболевания и приведёт к созданию лекарства от болезни. Новость об iPS-клетках приветствовали даже такие противники использования эмбриональных стволовых клеток из этических соображений, как президент США Джордж Буш и Папа Римский. Несмотря на то, что на тот момент эти клетки не спасли ни одного больного, в 2012 году профессор Яманака Синъя был удостоен Нобелевской премии по физиологии и медицине.
Открытие iPS-клеток человека дало старт конкуренции на пути к реализации мечты о регенеративной медицине.
Первоначальный метод получения вызывал опасения в связи с превращением клеток в раковые, к тому же эффективность производства была крайне низкой, но благодаря пересмотру техники получения, а также используемых генов, безопасность удалось повысить, и в результате в 2014 году приступили к клиническому испытанию. Двенадцатого сентября в больнице Центра передовой медицины Общества распространения передовой медицины (расположен в городе Кобэ) в глаз 70-летней женщины, страдающей от тяжёлой болезни зрения – дегенерациии (экссудативной) жёлтого пятна – были пересажены ткани пигментного эпителия сетчатки, выращенные с помощью iPS-клеток из кожных клеток самой пациентки.
Исследования возглавил офтальмолог Такахаси Масаё, руководитель проекта Института физико-химических исследований (RIKEN). Основной целью эксперимента была оценка безопасности – учёные намереваются убедиться в приживаемости клеток, а также в наличии либо отсутствии преобразований в раковые клетки более четырёх лет спустя после трансплантации. По прошествии двух лет после операции никаких проблем не возникло. Однако в ходе подготовки к запланированной на 2015 год операции на втором глазу пациентки в ряде iPS-клеток, произведённых из материала пациента, был обнаружен ряд генетических отклонений, в связи с чем от её проведения пришлось отказаться.
Стволовые клетки — панацея XXI века
* — Стволовые клетки можно получать и другими способами: ими может безо всякого ущерба для развития поделиться эмбрион («Щадящие стволовые клетки» [2]) или. его обиталище («Эндометрий как альтернативный источник стволовых клеток» [3]). — Ред.
** — О ситуации в области создания искусственных органов и технологиях их получения рассказывает статья «Органы из лаборатории» [4]. — Ред.
Помимо этого, впервые открываются возможности лечения генетических заболеваний. Молекулярная биология также не стоит на месте: разрабатывается огромное количество методов, позволяющих редактировать геном*, исправлять в нём «ошибки» или вносить дополнительные элементы. Но все эти методы малоэффективны применительно ко взрослому организму — дифференцировка его клеток, формирование органов и тканей происходили под влиянием причинных мутации. Чем же могут помочь ИПСК? Эти клетки представляют собой начальную форму клеточного развития. При коррекции генома на данной стадии последующая дифференцировка пройдет без отклонений.
* — Сейчас при разработке генотерапевтических подходов особые надежды возлагают на системы редактирования ZFN, TALEN и CRISPR/Cas9, основанные на сайт-специфическом действии нуклеаз in vivo. Эти системы обычно состоят из двух модулей, один из которых распознает нужную олигонуклеотидную последовательность, а другой режет цепи ДНК: «А не замахнуться ли нам на. изменение генома?» [5], «CRISPR-системы: иммунизация прокариот» [6]. И некоторые из подходов уже вполне «осязаемы», раз громче звучат голоса биоэтиков: «Мутагенная цепная реакция: редактирование геномов на грани фантастики» [7]. — Ред.
Прогресс в применении iPS-клеток для создания новых лекарств
Большие надежды с самого начала возлагаются и на второе основное направление использования – создание новых лекарственных препаратов.
Говорят, что доля веществ, которые оказываются пригодны к созданию лекарства, среди прочих подобных составляет не более одного на несколько десятков тысяч, при этом во многих случаях разработчики сталкиваются на полпути с возникновением тяжёлых побочных эффектов, вынуждающих начинать пробы с самого начала. iPS-клетки способны выступать в качестве инструмента, с помощью которого побочные эффекты можно спрогнозировать заранее. К примеру, воспользовавшись клетками печени, полученными путём преобразования iPS-клеток, можно заранее предвидеть печёночную токсичность. Кроме того, среди побочных эффектов следует выделить аритмию, угрожающую самой жизни пациента. Предсказать этот эффект становится возможным с использованием тканей сердечной мышцы, полученных преобразованием iPS-клеток.
Большие ожидания связаны и с областью трудноизлечимых заболеваний. В 2012 году Министерство образования, культуры, спорта, науки и технологий, а также Министерство здравоохранения, труда и благосостояния приступили к реализации научно-производственного проекта, направленного на борьбу с трудноизлечимыми заболеваниями, с использованием iPS-клеток. Он состоит в том, чтобы брать у пациента с трудноизлечимым заболеванием клетки организма – кожи, крови и т. д., получать в пяти центрах совместных исследований, в том числе в Киотском университете, iPS-клетки, изменённые заболеванием, и устанавливать природу заболевания, наблюдая за их преобразованиями в больные ткани, что может привести к созданию лекарства для излечения болезни. В сотрудничестве с 50 группами исследователей трудноизлечимых болезней при Министерстве здравоохранения, труда и социального обеспечения участие в проекте принимают 7 фармацевтических компаний.
Для практической реализации методов лечения с использованием iPS-клеток правительство выделяет десятки миллиардов йен, однако всё ещё остаются задачи в плане подготовки кадров. В научных кругах японской регенеративной медицины начала действовать система лицензирования для «врачей-специалистов регенеративной медицины» и «специалистов по клиническому выращиванию клеточных культур». Таким образом, за подготовку кадров, владеющих технологиями производства и обработки клеточных материалов, взялись всерьёз.
Если уже можно констатировать, что за прошедшее десятилетие удалось приступить к клиническим исследованиям iPS-клеток, вместе с тем необходимо признать, что до того времени, когда ими сможет воспользоваться любой нуждающийся, ещё предстоит пройти долгий путь. Но ученые по всему миру, во главе с пионером в этой области, профессором Яманака Синъя, верят в возможности iPS-клеток и не жалеют усилий в их исследованиях, стремясь сбалансировать скорость и безопасность, риски и выгоды использования.
Фото к заголовку: исследователь ставит опыт в открытой лаборатории Центра исследований iPS-клеток Киотского университета (фотография предоставлена Центром)

Новость
Колонии человеческих индуцированных плюрипотентных стволовых клеток (ИПСК) человека, полученные из клеток кожи
William Collins, Gladstone Institutes
Автор
Редакторы
Эмбриологи в первой половине XX века считали, что клетка — она как человек: в «детстве» (недифференцированном состоянии) все дороги открыты, а «взрослой» специализированной клетке обратного пути уже нет. В 2012 году Нобелевская премия по физиологии и медицине вручена за опровержение этой догмы: Джон Гардон и Шинья Яманака награждены «за открытие факта, что зрелые клетки могут быть „перепрограммированы“ обратно в плюрипотентное состояние».
Нобелевскую премию по физиологии и медицине в 2012 году получили Джон Гардон (John B. Gurdon) и Шинья Яманака (Shinya Yamanaka) «за открытие факта, что зрелые клетки могут быть „перепрограммированы“ обратно в плюрипотентное состояние». Их открытие продолжает ряд исследований, опровергающих догмы: ранее считалось, что процесс клеточной дифференциации — это «билет в один конец», и клетки, обретшие специализацию, уже никогда не могут вернуться в первичное состояние, когда все пути к дифференциации в различные клеточные линии еще открыты. (Такое состояние называют плюрипотентным.) В 1962 году британский биолог развития Гардон заложил первый камень в фундамент нового здания, показав, что пересадка ядра эпителиальной клетки взрослой лягушки в икринку, лишенную клеточного ядра, успешно дает начало нормальному головастику, в свою очередь развивающемуся во взрослую лягушку. Это исследование стало предтечей более поздних экспериментов по клонированию животных.
Однако все еще было непонятно, можно ли целую клетку также заставить «де-дифференцироваться», а потом — превратиться в любую из множества других специализированных клеток. В 2006 году положительный ответ на этот вопрос дал японец Шинья Яманака, использовавший небольшой набор транскрипционных факторов для такого «перепрограммирования». Полученные им клетки получили название индуцированных плюрипотентных стволовых клеток (ИПСК).
Оба этих открытия показали, что казавшееся незыблемым состояние дифференциации при «умелом» воздействии вполне можно отменить и полностью изменить тот путь, по которому предстоит развиваться клетке. Работы этих ученых открыли баснословные перспективы в биологии и медицине.
Ключ к дальнейшему прогрессу – предотвратить отторжение и превращение в раковые клетки
Преимущество использования материала самого пациента для получения iPS-клеток состоит в том, что этот подход позволяет ослабить реакцию отторжения, от которой зависит судьба трансплантации. Однако для первого пациента процесс получения из клеток пациента iPS-клеток, а также их последующая культивация и производство ткани сетчатки при тщательном контроле безопасности заняли в общей сложности 11 месяцев, а затраты разбухли до сотен миллионов йен. В связи с этим в следующий раз в RIKEN для получения клеток сетчатой оболочки глазного яблока, которые будут пересажены пациенту, рассчитывают воспользоваться запасом iPS-клеток исследовательского центра Киотского университета. С таким подходом возобновить трансплантации планируют в 2017 году.
Подобно группам крови, клетки разделяются по типам, образуя так называемую систему лейкоцитарных антигенов человека (HLA). Подобно тому, как кровь первой группы может быть перелита любому человеку, существуют группы клеток, не вызывающих реакции отторжения при пересадке любому другому человеку. В Киотском университете занимаются созданием запаса таких iPS-клеток высокой универсальности.

Ёмкости для хранения запаса iPS-клеток в научно-производственном отделе (FiT) Центра исследований iPS-клеток Киотского университета (фотография предоставлена Центром)
Даже при предположительном существовании нескольких десятков тысяч типов лейкоцитарных антигенов, унаследовавшие от родителей лейкоцитарные антигены одного типа люди формируют группы по типу АА, BB, CC. И если, к примеру, человеку с типом АА пересадить клетки от человека типа AB или AC, реакция отторжения будет минимальной. Среди японцев наиболее часто встречающиеся 75 типов лейкоцитарных антигенов охватывают 80% населения, а 140 типов покрывают 90% жителей. Такие масштабы позволяют создать в Киотском университете достаточный запас материала. Заручившись сотрудничеством Японского Красного креста, Банка пуповинной крови и других организаций, к людям с определёнными типами лейкоцитарных антигенов обращаются с просьбой стать донорами.
В Киотском университете из полученного таким образом донорского материала изготавливают высококачественные iPS-клетки, пригодные для лечения. Ожидается, что примерно к концу 2017 финансового года будет создан запас, охватывающий по пригодности 30-50% японцев.
С самого начала важнейшей технологической задачей являлось решение проблемы преобразования в раковые клетки. Даже сейчас, после перехода к новым методам получения, нельзя утверждать, что этот риск сведён к нулю. Когда iPS-клетки удаётся стимулировать к полному преобразованию в необходимый клеточный материал, проблем не возникает. Но если в процессе часть клеток остаются необращёнными, они могут привести к развитию опухоли. Ключом к успеху регенеративной медицины служит разработка метода, позволяющего либо обеспечивать полное преобразовние, либо дающего возможность избавляться от материала, не соответствующего поставленной задаче.
Эра перепрограммированных клеток
Гардон наглядно доказал, что перенос ядра в окружение раннего эмбрионального развития способен «перезапустить» программу развития. Однако можно ли такое сделать, не извлекая ядро из клетки? Многие ученые продолжали считать это невозможным, полагая эпигенетические изменения, произошедшие в дифференцированной клетке, слишком далеко зашедшими, чтобы можно было их обратить вспять. Наверное, так считал и Яманака, когда он начал заниматься эмбриональными стволовыми клетками (ЭСК) [6], впервые выделенными и культивированными Мартином Эвансом (лауреатом Нобелевской премии по физиологии и медицине 2008 года [7]).
Лаборатория Яманаки работала над поиском факторов, поддерживающих в ЭСК программу плюрипотентности. Было найдено несколько десятков генов, активность которых в ЭСК была намного выше, чем в дифференцированных клетках, и, кроме того, уже открыли, что слияние ЭСК и специализированной клетки может дать две плюрипотентные клетки [8].
Вооруженная этим знанием, группа Яманаки внедрила в клетку (выбрали фибробласт) вектор с 24 генами, заставившими часть клеток дать колонии, подобные стволовым клеткам, и принялась по одному удалять гены из этого набора. В результате был установлен список из всего четырех генов, необходимых для «перепрограммирования» клетки: Myc, Oct3/4, Sox2 и Klf4 (рис. 3) [9]. Полученные клетки, названные Яманакой индуцированными плюрипотентными стволовыми клетками (ИПСК), получались в результате изобретенной процедуры с крайне низким выходом, но применяемые технологии селекции позволяют обнаружить даже одну перепрограммированную клетку на сотни тысяч. Далее последовала серия работ этой и других лабораторий, в которых исследователи оптимизировали состав перепрограммирующих факторов и способ введения вектора в клетку, чтобы повысить эффективность перепрограммирования и снизить вероятность образования опухолевых клеток в результате вызываемой метаморфозы [10].
Об этих и других работах в новой и новейшей истории исследований стволовых клеток «биомолекула» рассказывала в двух больших обзорах: «Была клетка простая, стала стволовая» [10] и «Ствол и ветки: стволовые клетки» [11].

Рисунок 3. Способ перепрограммирования специализированной клетки в стволовую. Начиная с набора 24 транскрипционных факторов и постепенно сужая этот перечень (1), Такахаши и Яманака установили, что всего четыре гена (Myc, Oct3/4, Sox2 и Klf4) могут преобразить фибробласт, вернув его в состояние плюрипотентности (2) [9]. Полученные ИПСК (3) могут давать начало тератомам, что используется как маркер плюрипотентной клетки, а также использоваться в технологии получения химерных мышей (традиционно, для этого использовали ЭСК [7]).
Открытие Яманаки — важнейшее фундаментальное открытие в биологии, поскольку именно оно впервые продемонстрировало, что дифференцированная клетка может снова вернуться в «детство» и стать плюрипотентной. Весьма простая технология получения ИПСК мгновенно была взята на вооружение сотнями лабораторий по всему миру.
Широкая сфера продвижения исследований и разработок новых методов лечения
В настоящее время исследования с целью применения iPS-клеток в разнообразных методах лечения сердечной недостаточности, повреждений спинного мозга, болезни Паркинсона и массы других заболеваний приближаются к переходу от испытаний на животных к клиническим испытаниям на людях.
Декан медицинского факультета Университета Кэйо Окано Хидэюки занимается переходом к практической реализации метода лечения повреждений спинного мозга. Поскольку при повреждениях спинного мозга в результате несчастных случаев и травм нарушение быстро приобретает хронический характер, на своевременное получение iPS-клеток из собственных тканей пациента нет времени. Поэтому в дело вступает упомянутый ранее запас iPS-клеток Киотского университета, которые планируется обращать в нервные стволовые клетки. В настоящее время работа продвигается с тем, чтобы выполнить первую трансплантацию человеку уже в 2017 финансовом году. Это открывает перспективу использования такого подхода и при лечении инсультов.
В то же время профессор Осакского университета Сава Ёсиюки ведёт работу, целью которой является лечение сердечной недостаточности методом пересадки к сердцу ткани сердечной мышцы, полученной из iPS-клеток.
В Киотском университете профессор Такахаси Дзюн занимается разработкой метода борьбы с трудноизлечимой болезнью Паркинсона, суть которого состоит в получении вырабатывающих допамин нервных клеток из iPS-клеток. Более того, чтобы решить проблему нехватки доноров крови в стареющем обществе, совместно с Японским обществом Красного креста ведётся работа по получению из iPS-клеток тромбоцитов и эритроцитов. Продвигается и реализация плана создания метода лечения раковых заболеваний посредством активизации клеток иммунной системы с использованием технологии iPS-клеток.
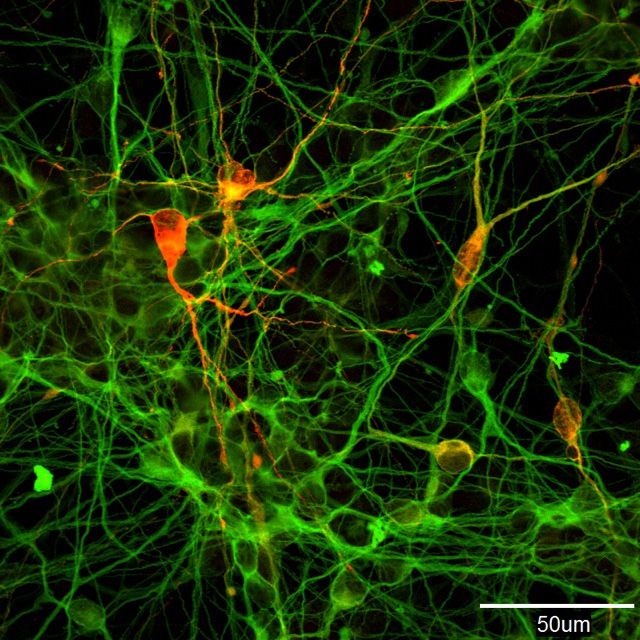
Клетки-производители допамина, полученные посредством инициации преобразования iPS-клеток человека (фотография предоставлена Моридзанэ Асука из Цетра исследований iPS-клеток Киотского университета)
Предпринимаются и попытки создания целых органов. Профессор Танигути Хидэки из Университета города Йокогама далеко продвинулся в создании объёмных элементов печени из клеток-прекурсоров (клеток, которые делятся и превращаются в клетки организма при его формировании).
Использование существующих препаратов контроля иммунитета в борьбе с трудноизлечимыми недугами
iPS-клетки – это клетки, способные преобразовываться в различные виды клеток организма (клетки мышц, костей, сердца, печени, кровеносных сосудов, нервной системы и т. д.), для получения которых достаточно воспользоваться клетками кожи, кровяными и некоторыми другими клетками. Со времени открытия iPS-клеток профессор Яманака наряду с регенеративной медициной отмечал в качестве одного из важнейших направлений клинического применения этих клеток создание лекарственных препаратов, и с сентября 2017 года начались клинические испытания медицинского препарата, предлагаемого в качестве лекарства от трудноизлечимого заболевания – прогрессирующей оссифицирующей фибродисплазии (FOP). Клинические испытания лекарства, открытого с использованием iPS-клеток, проводятся впервые в мире. Этим исследованием занимается заместитель руководителя Центра исследований iPS-клеток Киотского университета Тогутида Дзюнъя.
Прогрессирующая оссифицирующая фибродисплазия – трудноизлечимое генетическое заболевание, которое развивается с детского возраста. У больного по всему телу происходит преобразование в костные ткани грубоволокнистых соединительных тканей – мышц, сухожилий и связок, ограничивая подвижность суставов и деформируя кости. Человек лишается способности нормально питаться, затем затрудняется дыхание, и в конце концов больной умирает. Заболевание редкое – один случай на два миллиона человек, и в стране насчитывается порядка 80 человек с данным диагнозом. Учёные определили гены, вызывающие заболевание, однако эффективного метода его лечения не существует. Заболевание отнесено к числу недугов, лечение которых субсидируется государством.
Тогутида Дзюнъя использовал iPS-клетки, полученные из клеток пациентов с данным заболеванием, чтобы выявить вещества, подходящие в качестве лекарства, замедляющего развитие FOP. Сначала удалось добиться успеха в преобразовании взятых у пациента клеток в iPS-клетки. Путем сопоставления этих клеток со стандартными iPS-клетками удалось подтвердить воспроизводство заболевания FOP – заметно более высокую способность к преобразованию в костные и хрящевые клетки, и таким образом прояснить механизм аномального образования костных тканей у больного FOP. Затем, раз за разом наблюдая за реакцией этих iPS-клеток на воздействие различными соединениями, исследовав более 6 800 веществ, удалось обнаружить, что иммуносуппрессант рапамицин обладает нужным эффектом, подавляя преобразование в костные ткани.
Этот препарат используется в Европе для подавления реакции отторжения при проведении операций по пересадке органов (в Японии не одобрен), а в 2014 году препарат был одобрен в Японии в качестве средства для лечения редкого и трудноизлечимого заболевания – лимфангиолейомиоматоза. Такой метод использования уже существующего лекарственного средства в лечении совершенно иного заболевания, называемый переориентацией лекарства (DR), считается весьма безопасным ввиду отсутствия неизвестных побочных эффектов и т. п.
Нынешние клинические испытания, помимо Киотского университета, ведутся в больницах при Токийском университете, а также при университетах Нагои и Кюсю. Двадцать пациентов в возрасте от шести лет и старше разделили на две группы, в одной из которых на протяжении полугода пациенты получают рапамицин. Проверив таким образом его эффективность, исследователи ставят целью добиться одобрения этого препарата в качестве средства для лечения FOP.
Поскольку в случае переориентации уже существующего лекарственного средства проверки на безопасность для человеческого организма уже были проведены, а показатели фармакокинетики проверены на практике, это позволяет радикально снизить сумму издержек по сравнению с разработкой нового лекарства. Но ввиду того, что в случае трудноизлечимых заболеваний, которым подвержено небольшое число людей, фармацевтические компании не могут рассчитывать на получение прибыли, дело сложно довести и до проведения клинических испытаний – процесса, который обходится в сотни миллионов йен. Поэтому в таких случаях с целью расширить сферу применения существующих лекарств клинические испытания под руководством врачей финансируются из государственного бюджета.
Тем не менее.
Тем не менее некоторые ИПСК всё же добрались до применения на практике. Например, с их помощью начали лечить серповидноклеточную анемию*. ИПСК получали из клеток пациента и с помощью специализированных генетических методов исправляли мутацию, приводящую к этому заболеванию [11]. В конечном итоге ИПСК дифференцировали в здоровые эритроциты и вводили пациенту. Дело в том, что эритроциты — это тот редкий случай, когда непредсказуемая интеграция генов ТФ в клеточный геном не представляет никакой опасности, потому что в процессе дифференцировки эритроциты теряют ядро.
* — Генные и клеточные инженеры вообще неравнодушны к заболеваниям крови, и старания их приносят всё более ощутимые результаты — как по эффективности, так и по безопасности: «Сводка с генотерапевтических фронтов. Новая стратегия нейтрализации гемофилии» [12]. — Ред.
Упрощение клинических испытаний безопасности и эффективности
С помощью iPS-клеток, полученных от пациентов с определённым заболеванием (iPS-клеток с присущими заболеванию отличиями) становится возможным воспроизвести особое состояние клеток, характерное именно для данного недуга. Кроме того, это позволяет при проведении проверки лекарственного препарата на безопасность и эффективность не полагаться на опыты на животных, а проделывать необходимую работу, используя такие iPS-клетки.
Появляются надежды на создание лекарств не только для лечения FOP. В Университете Кэйо исследователи под руководством профессора Окано Хидэюки обнаружили препарат, который может послужить лекарством от бокового амиотрофического склероза (болезни Шарко), поражающего двигательные нейроны, и уже в 2018 году планируют приступить к клиническим испытаниям.
Кроме того, профессор Окано и его коллеги обнаружили, что рапамицин способен препятствовать отмиранию клеток внутреннего уха при наследственной глухоте (синдроме Пендреда). К тому же, группа под руководством профессора Фукуды Кэйити в Университете Кэйо обнаружила, что уже существующее лекарство, используемое для лечения лёгочной гипертензии, демонстрирует эффект при гипертрофической кардиомиопатии – наследственном заболевании, при котором происходит утолщение мышечных волокон сердца.

В Центре исследований iPS-клеток Киотского университета группа профессора Цумаки Нориюки обнаружила препарат, который, возможно, можно применять для трудноизлечимых костных заболеваний – хондродистрофии, при которой аномальное формирование клеток хрящевых тканей приводит к малорослости, а также танатофорной дисплазии. Это широко используемое по всему миру средство для понижения уровня холестерина – статин. Исследователи занимаются подтверждением его свойства восстанавливать рост костей.
Читайте также:


