Какое физическое явление лежит в основе работы однофотонного эмиссионного компьютерного томографа
Томография основана на получении послойных изображений объекта исследований. Впервые этот метод был разработан Н.И. Пироговым. Он создал атлас под названием "Топографическая анатомия", содержащий изображения послойных разрезов, проведённых через замороженное тело человека в трёх направлениях. Современная томография также основана на получении послойных изображений. Однако, современная томография позволяет проводить прижизненные исследования и с помощью математической обработки производить трехмерную реконструкцию изображения исследуемого органа.
В медицине используется различные методы томографии: Компьютерная томография (КТ), Магниторезонансная томография (МРТ), Однофотонная эмиссионная компьютерная томография (ОЭФКТ) и Позитронная эмиссионная томография (ПЭТ).
СОДЕРЖАНИЕ

Вместо того, чтобы просто «сфотографировать анатомические структуры», сканирование SPECT отслеживает уровень биологической активности в каждом месте анализируемой трехмерной области. Выбросы радионуклида указывают на количество кровотока в капиллярах визуализируемых областей. Точно так же, как обычный рентгеновский снимок представляет собой 2-мерный (2-D) вид трехмерной структуры, изображение, полученное с помощью гамма-камеры, является 2-мерным видом 3-мерного распределения радионуклида .
Визуализация SPECT выполняется с помощью гамма-камеры для получения нескольких двумерных изображений (также называемых проекциями ) под разными углами. Затем используется компьютер для применения алгоритма томографической реконструкции к нескольким проекциям, что дает набор трехмерных данных. Затем этим набором данных можно манипулировать, чтобы показать тонкие срезы вдоль любой выбранной оси тела, аналогичные тем, которые получены с помощью других томографических методов, таких как магнитно-резонансная томография (МРТ), рентгеновская компьютерная томография ( рентгеновская компьютерная томография ) и позитронно-эмиссионная томография (ПЭТ).
ОФЭКТ похожа на ПЭТ в использовании радиоактивного индикаторного материала и обнаружении гамма-лучей. В отличие от ПЭТ, индикаторы, используемые в ОФЭКТ, испускают гамма-излучение, которое измеряется напрямую, тогда как индикаторы ПЭТ испускают позитроны, которые аннигилируют с электронами на расстоянии до нескольких миллиметров, вызывая испускание двух гамма-фотонов в противоположных направлениях. Сканер ПЭТ обнаруживает эти выбросы «совпадающими» во времени, что дает больше информации о локализации событий излучения и, следовательно, изображения с более высоким пространственным разрешением, чем ОФЭКТ (разрешение около 1 см). Сканирование ОФЭКТ значительно дешевле, чем сканирование ПЭТ, отчасти потому, что оно позволяет использовать более долгоживущие и более легко получаемые радиоизотопы, чем ПЭТ.
Поскольку получение ОФЭКТ очень похоже на получение изображений с помощью планарной гамма-камеры, можно использовать те же радиофармпрепараты . Если пациент обследуется с помощью другого типа сканирования ядерной медицины, но изображения не являются диагностическими, можно сразу перейти к ОФЭКТ, переместив пациента к прибору ОФЭКТ или даже просто перенастроив камеру для получения изображения ОФЭКТ. пока пациент остается на столе.
Аппарат ОФЭКТ выполняет сканирование костей всего тела. Пациент лежит на столе, который скользит по аппарату, а пара гамма-камер вращается вокруг нее.
Для получения изображений SPECT гамма-камера вращается вокруг пациента. Проекции снимаются в определенных точках во время вращения, обычно каждые 3–6 градусов. В большинстве случаев для получения оптимальной реконструкции используется полное вращение на 360 градусов. Время, необходимое для получения каждого прогноза, также варьируется, но обычно 15–20 секунд. Это дает общее время сканирования 15–20 минут.
Гамма-камеры с несколькими головками могут ускорить получение. Например, двухголовая камера может использоваться с головками, разнесенными на 180 градусов друг от друга, что позволяет снимать две проекции одновременно, при этом каждая головка требует поворота на 180 градусов. Также используются тройные камеры с шагом 120 градусов.
Захват со стробированием сердца возможен с помощью ОФЭКТ, так же как и с помощью методов плоской визуализации, таких как сканирование с несколькими стробами (MUGA). Запущенная электрокардиограммой (ЭКГ) для получения дифференциальной информации о сердце в различных частях его цикла, закрытая ОФЭКТ миокарда может использоваться для получения количественной информации о перфузии миокарда, толщине и сократимости миокарда во время различных частей сердечного цикла, а также также для расчета фракции выброса левого желудочка , ударного объема и сердечного выброса.
ОФЭКТ можно использовать в качестве дополнения к любому исследованию гамма-визуализации, где может оказаться полезным истинное трехмерное изображение, например, при визуализации опухоли, инфекции ( лейкоцитов ), визуализации щитовидной железы или сцинтиграфии костей .
Поскольку ОФЭКТ обеспечивает точную локализацию в трехмерном пространстве, ее можно использовать для получения информации о локализованных функциях внутренних органов, например, функциональной визуализации сердца или головного мозга.
Визуализация перфузии миокарда (MPI) - это форма функциональной визуализации сердца, используемая для диагностики ишемической болезни сердца . Основной принцип заключается в том, что в условиях стресса больной миокард получает меньший кровоток, чем нормальный миокард. MPI - это один из нескольких видов сердечного стресс-теста .
Вводят специфический для сердца радиофармпрепарат, например 99m Tc- тетрофосмин (Myoview, GE healthcare), 99m Tc-сестамиби ( Cardiolite , Bristol-Myers Squibb) или хлорид таллия-201 . После этого частота сердечных сокращений увеличивается, чтобы вызвать стресс миокарда, либо упражнениями на беговой дорожке, либо фармакологически с аденозином , добутамином или дипиридамолом ( аминофиллин может использоваться для отмены эффектов дипиридамола).
Визуализация SPECT, выполненная после стресса, показывает распределение радиофармпрепарата и, следовательно, относительный кровоток в различных областях миокарда. Диагностика проводится путем сравнения стрессовых изображений с дополнительным набором изображений, полученных в состоянии покоя, которые обычно получают до стрессовых изображений.
Было продемонстрировано, что общая точность MPI составляет около 83% ( чувствительность : 85%; специфичность : 72%) (в обзоре, не только для SPECT MPI), [3] и сопоставима (или лучше) с другими не -инвазивные тесты на ишемическую болезнь сердца.
Обычно гамма-излучающий индикатор, используемый при функциональной визуализации мозга, представляет собой экзаметазим технеция (99mTc) . 99m Tc - это метастабильный ядерный изомер, который испускает гамма-лучи, обнаруживаемые с помощью гамма-камеры. Присоединение его к экзаметазиму позволяет ему поглощаться тканями мозга пропорционально мозговому кровотоку, что, в свою очередь, позволяет оценить церебральный кровоток с помощью ядерной гамма-камеры.
Поскольку кровоток в головном мозге тесно связан с локальным метаболизмом мозга и потреблением энергии, индикатор 99m Tc-экзаметазим (а также аналогичный индикатор 99m Tc-EC) используется для региональной оценки метаболизма мозга в попытке диагностировать и дифференцировать различные причинные патологии деменции . Метаанализ многих опубликованных исследований показывает, что чувствительность ОФЭКТ с этим индикатором составляет около 74% при диагностике болезни Альцгеймера по сравнению с чувствительностью 81% при клиническом обследовании ( когнитивное тестирование и т. Д.). Более поздние исследования показали, что точность ОФЭКТ в диагностике болезни Альцгеймера может достигать 88%. [4] В метаанализе ОФЭКТ превосходила клиническое обследование и клинические критерии (91% против 70%) в способности дифференцировать болезнь Альцгеймера от сосудистой деменции. [5] Эта последняя способность связана с визуализацией локального метаболизма головного мозга с помощью ОФЭКТ, при которой точечная потеря коркового метаболизма, наблюдаемая при множественных инсультах, явно отличается от более равномерной или «плавной» потери не затылочной корковой функции мозга, типичной для болезни Альцгеймера. болезнь. Другая недавняя обзорная статья показала, что многоголовые ОФЭКТ-камеры с количественным анализом дают общую чувствительность 84-89% и общую специфичность 83-89% в поперечных исследованиях, чувствительность 82-96% и специфичность 83-89 % для продольных исследований деменции. [6]
ОФЭКТ-сканирование с использованием 99m Tc-экзаметазима конкурирует с ПЭТ- сканированием на основе флудезоксиглюкозы (ФДГ) головного мозга, которое позволяет оценить региональный метаболизм глюкозы в головном мозге и предоставить очень похожую информацию о локальном повреждении мозга в результате многих процессов. ОФЭКТ более широко доступна, потому что используемый радиоизотоп более долговечен и намного дешевле в ОФЭКТ, а также менее дорогое оборудование для гамма-сканирования. В то время как 99m Tc извлекается из относительно простых генераторов технеция-99m , которые еженедельно доставляются в больницы и сканирующие центры для снабжения свежим радиоизотопом, FDG PET полагается на FDG, который производится на дорогостоящем медицинском циклотроне. и «горячая лаборатория» (автоматизированная химическая лаборатория для производства радиофармпрепаратов), а затем немедленно доставляется в места сканирования из-за естественного короткого периода полураспада фтора-18, составляющего 110 минут .
В ядерной энергетике метод SPECT может применяться для визуализации распределения радиоизотопов в облученном ядерном топливе. [7] Из-за облучения ядерного топлива (например, урана) нейтронами в ядерном реакторе, в топливе естественным образом образуется широкий спектр гамма-излучающих радионуклидов, таких как продукты деления ( цезий-137 , барий-140 и европий). -154 ) и продуктов активации ( хром-51 и кобальт-58 ). Их можно отобразить с помощью ОФЭКТ, чтобы проверить наличие топливных стержней в хранимой топливной сборке для целей гарантий МАГАТЭ [8], чтобы подтвердить прогнозы кодов моделирования активной зоны, [9] или изучить поведение ядерного топлива при нормальной эксплуатации [10] или в аварийных сценариях. [11]

Восстановленные изображения обычно имеют разрешение 64 × 64 или 128 × 128 пикселей с размером пикселей в диапазоне 3–6 мм. Количество полученных проекций выбирается примерно равным ширине получаемых изображений. Как правило, полученные восстановленные изображения будут иметь более низкое разрешение, будут иметь повышенный шум, чем плоские изображения, и будут подвержены артефактам .
Сканирование занимает много времени, и очень важно, чтобы во время сканирования пациент не двигался. Движение может вызвать значительное ухудшение восстановленных изображений, хотя методы восстановления с компенсацией движения могут помочь в этом. Крайне неравномерное распределение радиофармпрепарата также может вызвать артефакты. Очень интенсивная область активности (например, мочевой пузырь) может вызвать появление обширных полос на изображениях и затемнить соседние области активности. Это ограничение алгоритма реконструкции отфильтрованной обратной проекции . Итерационная реконструкция - это альтернативный алгоритм, важность которого растет, поскольку он менее чувствителен к артефактам и может также корректировать затухание и размытие, зависящее от глубины. Кроме того, итерационные алгоритмы могут быть сделаны более эффективным использованием Superiorization методологии. [12]
Рассеяние гамма-лучей, а также случайный характер гамма-лучей также могут привести к ухудшению качества изображений SPECT и вызвать потерю разрешения. Коррекция рассеяния и восстановление разрешения также применяются для улучшения разрешения изображений SPECT. [13]
В некоторых случаях гамма-сканер SPECT может быть построен для работы с обычным компьютерным томографом с одновременной регистрацией изображений. Как и в ПЭТ / КТ , это позволяет определять местонахождение опухолей или тканей, которые можно увидеть на сцинтиграфии ОФЭКТ, но которые трудно точно определить относительно других анатомических структур. Такое сканирование наиболее полезно для тканей за пределами мозга, где расположение тканей может быть гораздо более изменчивым. Например, ОФЭКТ / КТ может использоваться в приложениях сканирования паращитовидных желез сестамиби , где этот метод полезен для обнаружения эктопических аденом паращитовидных желез, которые могут находиться не на своих обычных местах в щитовидной железе. [14]
Общие характеристики систем SPECT могут быть выполнены с помощью инструментов контроля качества, таких как фантом Ящака . [15]
Однофотонная эмиссионная компьютерная томография ( ОФЭКТ или, реже, СПЭТ ) - это метод томографической визуализации ядерной медицины с использованием гамма-лучей . [1] Это очень похоже на обычную плоскую визуализацию в ядерной медицине с использованием гамма-камеры (то есть сцинтиграфию ), [2] но способно предоставить истинную трехмерную информацию. Эта информация обычно представлена в виде срезов пациента, но при необходимости ее можно свободно переформатировать или изменять.
Этот метод требует доставки пациенту гамма-излучающего радиоизотопа ( радионуклида ), обычно путем инъекции в кровоток. Иногда радиоизотоп представляет собой простой растворимый растворенный ион, такой как изотоп галлия (III). Однако в большинстве случаев радиоизотоп-маркер присоединяется к определенному лиганду для создания радиолиганда , свойства которого связывают его с определенными типами тканей. Это сочетание позволяет переносить комбинацию лиганда и радиофармпрепарата и связывать ее с интересующим местом в организме, где концентрация лиганда определяется гамма-камерой.

Вместо того, чтобы просто «сфотографировать анатомические структуры», сканирование SPECT отслеживает уровень биологической активности в каждом месте анализируемой трехмерной области. Выбросы радионуклида указывают на количество кровотока в капиллярах визуализируемых областей. Точно так же, как обычный рентгеновский снимок представляет собой 2-мерный (2-D) вид трехмерной структуры, изображение, полученное с помощью гамма-камеры, является 2-мерным видом 3-мерного распределения радионуклида .
ОФЭКТ-визуализация выполняется с помощью гамма-камеры для получения нескольких двумерных изображений (также называемых проекциями ) под разными углами. Затем компьютер используется для применения алгоритма томографической реконструкции к множеству проекций, что дает набор трехмерных данных. Затем этим набором данных можно манипулировать, чтобы показать тонкие срезы вдоль любой выбранной оси тела, аналогичные тем, которые получены с помощью других томографических методов, таких как магнитно-резонансная томография (МРТ), рентгеновская компьютерная томография (рентгеновская КТ) и позитронно-эмиссионная томография (ПЭТ).
ОФЭКТ похожа на ПЭТ в использовании радиоактивного индикаторного материала и обнаружении гамма-лучей. В отличие от ПЭТ, индикаторы, используемые в ОФЭКТ, испускают гамма-излучение, которое измеряется напрямую, тогда как индикаторы ПЭТ испускают позитроны, которые аннигилируют с электронами на расстоянии до нескольких миллиметров, вызывая испускание двух гамма-фотонов в противоположных направлениях. Сканер ПЭТ обнаруживает эти выбросы, «совпадающие» во времени, что дает больше информации о локализации событий излучения и, следовательно, изображения с более высоким пространственным разрешением, чем ОФЭКТ (разрешение около 1 см). ОФЭКТ-сканирование значительно дешевле, чем ПЭТ-сканирование, отчасти потому, что они могут использовать более долгоживущие и более легко получаемые радиоизотопы, чем ПЭТ.
Поскольку получение ОФЭКТ очень похоже на получение изображений с помощью планарной гамма-камеры, можно использовать те же радиофармпрепараты . Если пациент обследуется с помощью другого типа сканирования ядерной медицины, но изображения не являются диагностическими, можно сразу перейти к ОФЭКТ, переместив пациента к прибору ОФЭКТ или даже просто перенастроив камеру для получения изображения ОФЭКТ. пока пациент остается на столе.
Аппарат ОФЭКТ выполняет сканирование костей всего тела. Пациент лежит на столе, который скользит по аппарату, а пара гамма-камер вращается вокруг нее.
Для получения изображений SPECT гамма-камера вращается вокруг пациента. Проекции снимаются в определенных точках во время вращения, обычно каждые 3–6 градусов. В большинстве случаев для получения оптимальной реконструкции используется полное вращение на 360 градусов. Время, необходимое для получения каждого прогноза, также варьируется, но обычно 15–20 секунд. Это дает общее время сканирования 15–20 минут.
Гамма-камеры с несколькими головками могут ускорить получение. Например, двухголовая камера может использоваться с головками, разнесенными на 180 градусов друг от друга, что позволяет снимать две проекции одновременно, при этом каждая головка требует поворота на 180 градусов. Также используются тройные камеры с шагом 120 градусов.
Захват со стробированием сердца возможен с помощью ОФЭКТ, так же как и с помощью методов плоской визуализации, таких как сканирование с несколькими стробами (MUGA). Запущенная электрокардиограммой (ЭКГ) для получения дифференциальной информации о сердце в различных частях его цикла, закрытая ОФЭКТ миокарда может использоваться для получения количественной информации о перфузии миокарда, толщине и сократимости миокарда во время различных частей сердечного цикла, а также также для расчета фракции выброса левого желудочка , ударного объема и сердечного выброса.
ОФЭКТ можно использовать в качестве дополнения к любому исследованию гамма-визуализации, где может оказаться полезным истинное трехмерное изображение, например, при визуализации опухоли, инфекции ( лейкоцитов ), визуализации щитовидной железы или сцинтиграфии костей .
Поскольку ОФЭКТ обеспечивает точную локализацию в трехмерном пространстве, ее можно использовать для получения информации о локализованных функциях внутренних органов, например, функциональной визуализации сердца или головного мозга.
Однофотонная эмиссионная компьютерная томография
(Single-photon emission computed tomography, SPECT)
Дальнейшее развитие радиоизотопной диагностики привело к созданию однофотонных эмиссионных компьютерных томографов (ОФЭКТ). В этих томографах трехмерное изображение получается путём компьютерной обработки серии плоскостных сцинтиграмм.
Для того, чтобы получить изображения в ОФЭКТ, гамма-камера поворачивается вокруг пациента. Проекции фиксируются, как правило, через каждые 3-6 градусов. В большинстве случаев для получения оптимального восстановления, используется полное вращение на 360 градусов. Типичное время, необходимое для получения каждой проекции 15-20 секунд. Соответственно общее время сканирования 15-20 минут. Для уменьшения времени сканирования используются детектирующие системы состоящие из двух или более гамма-камер.
Использование электрокардиографа в качества триггера в ОФЭКТ позволяет получить дифференциальную информацию о работе сердца в различные моменты сердечного цикла.
В сцинтиграфии и ОФЭКТ используются одни и те же радиоактивные препараты. В большинстве диагностических процедур (~80%) в течение последних 30 лет используются препараты с 99m Tc. Однако используют и другие радиоизотопы. В таблице приведены некоторые изотопы, используемые в диагностике
Так для сцинтиграфии сердца используют 201 Tl, пирофосфат 99m Тс, 67 Ga. Галлий, например, накапливается в воспалительных очагах в сердце, что проявляется на сцинтиграммах. При сцинтиграфии легких: с помощью альбумина, меченного 131 I или 99m Тс, на сцинтиграммах обнаруживают зоны значительного уменьшения накопления изотопа, что свидетельствует о тромбоэмболии легочной артерии. Изображение костного мозга можно получить с помощью серного коллоида, меченного технецием 99m Тс, который накапливается в клеточных элементах костного мозга. При острых лейкозах, у больных миелосклерозом, при лимфогранулематозе в изображениях костного мозга имеются особенности. Сцинтиграфия щитовидной железы проводится с помощью препаратов 131 I или 99m Тс, что позволяет диагностировать в ней узловые образования.
КТ + ОФЭКТ
Объединение компьютерной томографии и однофотонной эмиссионной компьютерной томографии в единой системе приводит к повышению точности обоих типов исследования. Так ослабление гамма-излучения, внутри пациента может привести к существенной недооценке активности в глубоких тканях, по сравнению с поверхностными тканями. Использование интегрированного с ОФЭКТ компьютерного томографа позволяет оптимизировать коррекцию поглощения гамма-излучения в тканях. Интегрированная система позволяет точно определить локализацию поражения при наложении изображения, проводить своевременную диагностику онкологических заболеваний, осуществлять дифференциацию злокачественных и доброкачественных образований различных органов и систем, выявлять наличие структурных изменений и функциональных нарушений на стадии минимальных клинических проявлений заболевания.
Функциональная томография головного мозга
Обычно гамма-излучающий индикатор, используемый при функциональной визуализации мозга, представляет собой экзаметазим технеция (99mTc) . 99m Tc - это метастабильный ядерный изомер, который испускает гамма-лучи, обнаруживаемые с помощью гамма-камеры. Присоединение его к экзаметазиму позволяет ему поглощаться тканями мозга пропорционально мозговому кровотоку, что, в свою очередь, позволяет оценить церебральный кровоток с помощью ядерной гамма-камеры.
Поскольку кровоток в головном мозге тесно связан с локальным метаболизмом мозга и потреблением энергии, индикатор 99m Tc-экзаметазим (а также аналогичный индикатор 99m Tc-EC) используется для региональной оценки метаболизма мозга в попытке диагностировать и дифференцировать различные причинные патологии деменции . Метаанализ многих опубликованных исследований показывает, что чувствительность ОФЭКТ с этим индикатором составляет около 74% при диагностике болезни Альцгеймера по сравнению с чувствительностью 81% при клиническом обследовании ( когнитивные тесты и т. Д.). Более поздние исследования показали, что точность ОФЭКТ в диагностике болезни Альцгеймера может достигать 88%. [4] В метаанализе ОФЭКТ превосходила клиническое обследование и клинические критерии (91% против 70%) в способности дифференцировать болезнь Альцгеймера от сосудистой деменции. [5] Эта последняя способность связана с визуализацией локального метаболизма головного мозга с помощью ОФЭКТ, при которой точечная потеря коркового метаболизма, наблюдаемая при множественных инсультах, явно отличается от более равномерной или «плавной» потери не затылочной корковой функции мозга, типичной для болезни Альцгеймера. болезнь. Другая недавняя обзорная статья показала, что многоголовые ОФЭКТ-камеры с количественным анализом дают общую чувствительность 84-89% и общую специфичность 83-89% в поперечных исследованиях, чувствительность 82-96% и специфичность 83-89 % для продольных исследований деменции. [6]
ОФЭКТ-сканирование с использованием 99m Tc-экзаметазима конкурирует с ПЭТ- сканированием на основе флудезоксиглюкозы (ФДГ) головного мозга, которое позволяет оценить региональный метаболизм глюкозы в головном мозге и предоставить очень похожую информацию о локальном повреждении мозга в результате многих процессов. ОФЭКТ более широко доступна, потому что используемый радиоизотоп более долговечен и намного дешевле в ОФЭКТ, а также менее дорогое оборудование для гамма-сканирования. В то время как 99m Tc извлекается из относительно простых генераторов технеция-99m , которые еженедельно доставляются в больницы и сканирующие центры для поставки свежего радиоизотопа, FDG PET полагается на FDG, который производится на дорогостоящем медицинском циклотроне и в «горячей лаборатории» (автоматизированная химия). лаборатории для производства радиофармпрепаратов), а затем немедленно доставили в места сканирования из-за естественного короткого периода полураспада фтора-18, составляющего 110 минут .
Компьютерная томография
Компьютерная томография — метод неразрушающего послойного исследования внутреннего строения был предложен в 1979 году Годфри Хаунсфилдом и Алланом Кормаком, удостоенных за эту разработку Нобелевской премии.
У обычных рентгеновских методов есть недостатки. Во-первых, в двумерной рентгеновской картине объекты расположены в глубине накладываться (см. рис.1). Во-вторых, обычно рентгеновские лучи не могут различать мягкие ткани. Изменения в мягких тканях, таких как печень и поджелудочная железа, не различимы, а некоторые другие органы могут быть сделаны видимыми только посредством использования рентгеноконтрастных красителей. В-третьих, при использовании обычных рентгеновских методов, не представляется возможным количественно измерить плотности отдельных веществ, через которые прошло рентгеновское излучение. Радиограмма фиксирует только среднее поглощение всех различных тканей. Компьютерная томография измеряет ослабление рентгеновских лучей, проходящих через участки тела из сотен различных углов, получая срезы, а затем, с помощью компьютерной обработки, большой серии двумерных рентгенографических снимков, сделанных вокруг одной оси вращения, получается трехмерное изображение.
Прогресс КТ-томографов напрямую связан с увеличением количества детекторов, то есть с увеличением числа одновременно собираемых проекций.
Аппарат 1-го поколения появился в 1973 году. КТ-аппараты первого поколения были пошаговыми. Была одна трубка, направленная на один детектор. Сканирование производилось шаг за шагом, делая по одному обороту на слой. Каждый слой обрабатывался около 4 минут.
Дальнейший прогресс связан с появлением
спиральных компьютерных томографов (1988 г.) и увеличением количества детекторов. Спиральное сканирование заключается в непрерывном вращении рентгеновской трубки и непрерывном поступательного движения стола с пациентом вдоль продольной оси сканирования z через апертуру гентри*. Технология спирального сканирования позволила значительно сократить время, затрачиваемое на КТ-исследование и существенно уменьшить лучевую нагрузку на пациента.
В 1992 г. появились первые мультисрезовые компьютерные томографы (МСКТ). В них по окружности гентри расположены не один, а два и более ряда детекторов. К 2013 г. количество срезов было доведено до 512 и 640. Для того, чтобы рентгеновское излучение могло одновременно приниматься детекторами, расположенными на разных рядах, была разработана новая — объёмная геометрическая форма пучка. Стали производиться томографы с двумя рентгеновскими трубками, расположенными под углом 90°, что позволило еще уменьшить временное разрешение.
Современные томографы позволяют не только получать изображения, но и дают возможность практически в «реальном» времени наблюдать физиологические процессы, происходящие в головном мозге и в сердце. Они дают возможность сканирования целого органа (сердце, суставы, головной мозг и т. д.) за один оборот рентгеновской трубки, что значительно сокращает время обследования, а также дает возможность для сканирования сердца даже у пациентов, страдающих аритмиями.
КТ на сегодняшний день - ведущий метод диагностики многих заболеваний головного мозга, позвоночника, легких и средостения, печени, почек, поджелудочной железы, надпочечников, аорты и легочной артерии, сердца и ряда других органов. КТ можно использовать и как метод первичной диагностики, и как уточняющую методику, когда предварительный диагноз уже поставлен с помощью УЗИ или клинического обследования.
МСКТ - это лучший метод диагностики заболеваний легких и костей скелета. При введении контрастного препарата КТ позволяет получать качественные трехмерные изображения сосудов и сердца, в том числе коронарных артерий и аортокоронарных шунтов. Для проведения этих исследований не требуется госпитализация и введение катетера в сосуды сердца.
Визуализация перфузии миокарда
Визуализация перфузии миокарда (MPI) - это форма функциональной визуализации сердца, используемая для диагностики ишемической болезни сердца . Основной принцип заключается в том, что в условиях стресса больной миокард получает меньший кровоток, чем нормальный миокард. MPI - это один из нескольких видов сердечного стресс-теста .
Вводят специфический для сердца радиофармпрепарат, например 99m Tc- тетрофосмин (Myoview, GE healthcare), 99m Tc-сестамиби ( Cardiolite , Bristol-Myers Squibb) или хлорид таллия-201 . После этого частота сердечных сокращений увеличивается, чтобы вызвать стресс миокарда, либо упражнениями на беговой дорожке, либо фармакологически с аденозином , добутамином или дипиридамолом ( аминофиллин может использоваться для отмены эффектов дипиридамола).
Визуализация SPECT, выполненная после стресса, показывает распределение радиофармпрепарата и, следовательно, относительный кровоток в различных областях миокарда. Диагностика проводится путем сравнения стрессовых изображений с дополнительным набором изображений, полученных в состоянии покоя, которые обычно получают до стрессовых изображений.
Было продемонстрировано, что общая точность MPI составляет около 83% ( чувствительность : 85%; специфичность : 72%) (в обзоре, не только для SPECT MPI), [3] и сопоставима (или лучше) с другими не -инвазивные тесты на ишемическую болезнь сердца.
Компьютерная томография
Компьютерная томография — метод неразрушающего послойного исследования внутреннего строения был предложен в 1979 году Годфри Хаунсфилдом и Алланом Кормаком, удостоенных за эту разработку Нобелевской премии.
У обычных рентгеновских методов есть недостатки. Во-первых, в двумерной рентгеновской картине объекты расположены в глубине накладываться (см. рис.1). Во-вторых, обычно рентгеновские лучи не могут различать мягкие ткани. Изменения в мягких тканях, таких как печень и поджелудочная железа, не различимы, а некоторые другие органы могут быть сделаны видимыми только посредством использования рентгеноконтрастных красителей. В-третьих, при использовании обычных рентгеновских методов, не представляется возможным количественно измерить плотности отдельных веществ, через которые прошло рентгеновское излучение. Радиограмма фиксирует только среднее поглощение всех различных тканей. Компьютерная томография измеряет ослабление рентгеновских лучей, проходящих через участки тела из сотен различных углов, получая срезы, а затем, с помощью компьютерной обработки, большой серии двумерных рентгенографических снимков, сделанных вокруг одной оси вращения, получается трехмерное изображение.
Прогресс КТ-томографов напрямую связан с увеличением количества детекторов, то есть с увеличением числа одновременно собираемых проекций.
Аппарат 1-го поколения появился в 1973 году. КТ-аппараты первого поколения были пошаговыми. Была одна трубка, направленная на один детектор. Сканирование производилось шаг за шагом, делая по одному обороту на слой. Каждый слой обрабатывался около 4 минут.
Дальнейший прогресс связан с появлением
спиральных компьютерных томографов (1988 г.) и увеличением количества детекторов. Спиральное сканирование заключается в непрерывном вращении рентгеновской трубки и непрерывном поступательного движения стола с пациентом вдоль продольной оси сканирования z через апертуру гентри*. Технология спирального сканирования позволила значительно сократить время, затрачиваемое на КТ-исследование и существенно уменьшить лучевую нагрузку на пациента.
В 1992 г. появились первые мультисрезовые компьютерные томографы (МСКТ). В них по окружности гентри расположены не один, а два и более ряда детекторов. К 2013 г. количество срезов было доведено до 512 и 640. Для того, чтобы рентгеновское излучение могло одновременно приниматься детекторами, расположенными на разных рядах, была разработана новая — объёмная геометрическая форма пучка. Стали производиться томографы с двумя рентгеновскими трубками, расположенными под углом 90°, что позволило еще уменьшить временное разрешение.
Современные томографы позволяют не только получать изображения, но и дают возможность практически в «реальном» времени наблюдать физиологические процессы, происходящие в головном мозге и в сердце. Они дают возможность сканирования целого органа (сердце, суставы, головной мозг и т. д.) за один оборот рентгеновской трубки, что значительно сокращает время обследования, а также дает возможность для сканирования сердца даже у пациентов, страдающих аритмиями.
КТ на сегодняшний день - ведущий метод диагностики многих заболеваний головного мозга, позвоночника, легких и средостения, печени, почек, поджелудочной железы, надпочечников, аорты и легочной артерии, сердца и ряда других органов. КТ можно использовать и как метод первичной диагностики, и как уточняющую методику, когда предварительный диагноз уже поставлен с помощью УЗИ или клинического обследования.
МСКТ - это лучший метод диагностики заболеваний легких и костей скелета. При введении контрастного препарата КТ позволяет получать качественные трехмерные изображения сосудов и сердца, в том числе коронарных артерий и аортокоронарных шунтов. Для проведения этих исследований не требуется госпитализация и введение катетера в сосуды сердца.
Применения в ядерной технологии
В ядерной энергетике метод SPECT может применяться для визуализации распределения радиоизотопов в облученном ядерном топливе. [7] Из-за облучения ядерного топлива (например, урана) нейтронами в ядерном реакторе, в топливе естественным образом образуется широкий спектр гамма-излучающих радионуклидов, таких как продукты деления ( цезий-137 , барий-140 и европий). -154 ) и продуктов активации ( хром-51 и кобальт-58 ). Их можно получить с помощью ОФЭКТ, чтобы проверить наличие топливных стержней в хранимой топливной сборке для целей гарантий МАГАТЭ [8], чтобы подтвердить прогнозы кодов моделирования активной зоны [9] или изучить поведение ядерного топлива в нормальных условиях. эксплуатации, [10] или в аварийных сценариях. [11]

Восстановленные изображения обычно имеют разрешение 64 × 64 или 128 × 128 пикселей с размером пикселей в диапазоне 3–6 мм. Количество полученных проекций выбирается примерно равным ширине получаемых изображений. Как правило, полученные восстановленные изображения будут иметь более низкое разрешение, будут иметь повышенный шум, чем плоские изображения, и будут подвержены артефактам .
Сканирование занимает много времени, и очень важно, чтобы во время сканирования пациент не двигался. Движение может вызвать значительное ухудшение восстановленных изображений, хотя методы восстановления с компенсацией движения могут помочь в этом. Крайне неравномерное распределение радиофармпрепарата также может вызвать артефакты. Очень интенсивная область активности (например, мочевой пузырь) может вызвать появление обширных полос на изображениях и затемнить соседние области активности. Это ограничение алгоритма реконструкции отфильтрованной обратной проекции . Итеративная реконструкция - это альтернативный алгоритм, важность которого растет, поскольку он менее чувствителен к артефактам и может также корректировать затухание и размытие, зависящее от глубины. Кроме того, итерационные алгоритмы могут быть сделаны более эффективным использованием Superiorization методологии. [12]
Рассеяние гамма-лучей, а также случайный характер гамма-лучей также могут привести к ухудшению качества изображений SPECT и вызвать потерю разрешения. Коррекция рассеяния и восстановление разрешения также применяются для улучшения разрешения изображений SPECT. [13]
| Изучение | Радиоизотоп | Энергия излучения (кэВ) | Период полураспада | Радиофармпрепараты | Активность ( МБк ) | Вращение (градусы) | Прогнозы | Разрешение изображения | Время на проекцию (с) |
|---|---|---|---|---|---|---|---|---|---|
| Рентген | технеций-99m | 140 | 6 часов | Фосфонаты / бисфосфонаты | 800 | 360 | 120 | 128 х 128 | 30 |
| Сканирование перфузии миокарда | технеций-99m | 140 | 6 часов | тетрофосмин; Сестамиби | 700 | 180 | 60 | 64 х 64 | 25 |
| Сканирование паращитовидных желез Sestamibi | технеций-99m | 140 | 6 часов | Сестамиби | |||||
| Сканирование мозга | технеций-99m | 140 | 6 часов | Tc exametazime; ECD | 555-1110 | 360 | 64 | 128 х 128 | 30 |
| Нейроэндокринное или неврологическое сканирование опухолей | йод-123 или йод-131 | 159 | 13 часов или 8 дней | MIBG | 400 | 360 | 60 | 64 х 64 | 30 |
| Сканирование белых клеток | индий-111 и технеций-99m | 171 и 245 | 67 часов | лейкоциты, меченные in vitro | 18 | 360 | 60 | 64 х 64 | 30 |
В некоторых случаях гамма-сканер SPECT может быть построен для работы с обычным компьютерным томографом с одновременной регистрацией изображений. Как и в ПЭТ / КТ , это позволяет определять местонахождение опухолей или тканей, которые можно увидеть на сцинтиграфии ОФЭКТ, но которые трудно точно определить относительно других анатомических структур. Такое сканирование наиболее полезно для тканей за пределами мозга, где расположение тканей может быть гораздо более изменчивым. Например, ОФЭКТ / КТ может использоваться в приложениях сканирования паращитовидных желез сестамиби , где этот метод полезен для обнаружения эктопических аденом паращитовидных желез, которые могут находиться не на своих обычных местах в щитовидной железе. [14]
Общие характеристики систем SPECT могут быть выполнены с помощью инструментов контроля качества, таких как фантом Ящака . [15]
Сцинтиграфия и однофотонная эмиссионная компьютерная томография
Сцинтиграфия
Сцинтиграфия — метод функциональной визуализации, заключающийся во введении в организм радиоактивных изотопов и получении двумерного изображения путём определения испускаемого ими излучения.
Пациенту вводят препарат, состоящий из молекулы-вектора и радионуклида*. Молекула-вектор поглощается определённой структурой организма (орган, ткань, жидкость). Радионуклид излучает, и его излучение регистрируется детектором (гамма-камерой).
В состав современной гамма-камеры входят (см. рис. 3)
- многоканальный коллиматор, выделяющий направление гамма-квантов;
- сцинтиллятор большой площади
(~ 60×45 см); - матрица из ФЭУ;
- электроника, с помощью которой извлекается информация о координатах и интенсивности сцинилляции;
- ЭВМ, в котором строится сцинтиграфическое двумерное изображение исследуемого органа.
Чтобы получить информацию о направлении вылета из человеческого тела γ-квантов, происходит их коллимация в многоканальном коллиматоре. Сцинтиллятор детектора просматривается матрицей фотоумножителей. Таким образом определяется направление прихода γ-кванта, что дает возможность реконструировать точку его испускания.
Позитронно-эмиссионная томография
(Двухфотонная эмиссионная томография)
ПЭТ сегодня является одним из самых совершенных диагностических инструментов.
Рентгеновская, ультразвуковая, и магнитно-резонасная томография проявляют структуру органа на стадии её патологического изменения. ПЭТ же способен зарегистрировать изменения в обменных процессах, которые этому предшествуют. ПЭТ помогает самому раннему распознаванию патологических сдвигов задолго до появления морфологических изменений. ПЭТ применяется в онкологии, кардиологии и неврологии, при изучении метаболических процессов в мозге и других органах, механизмов действия лекарственных препаратов. Возможности ПЭТ в значительной степени определяется арсеналом доступных меченых соединений — радиофармпрепаратов (РФП).
Рассмотрим принцип работы ПЭТ.
Пациенту вводят РФП, содержащий β + -активный изотоп.
Позитроны, испущенные радионуклидами, имеют в биологических тканях очень короткий пробег (несколько мм). В результате аннигиляции позитронов образуются два γ-кванта с энергиями 511 кэВ. Таким образом, аннигиляция происходит практически в том же месте, где находилась молекула РФП. γ-Кванты разлетаются в противоположных направлениях и регистрируется методом совпадений. Пара датчиков располагается на одной прямой с различных сторон пациента, и оба γ-кванта попадают на свои датчики одновременно. В результате регистрации такого события можно построить прямую линию, проходящую через область концентрации радионуклида. Сегментированный детектор выполнен в виде нескольких колец, окружающих пациента см. рис. 6. Зарегистрировав большое число пар γ-квантов, и, построив пересечение их траекторий, можно получить изображение распределения РФП и таким образом визуализовать исследуемый орган.
В современных системах с высоким временным разрешением используется метод "время пролета", позволяющий с точностью нескольких сотен пикосекунд определить разницу во времени между обнаружением двух фотонов. Это позволяет локализовать место, где произошла аннигиляция в пределах десяти сантиметров. Этой точности недостаточно для ПЭТ, однако использование дополнительной информации, которую дает использование метода времени пролета позволяет при реконструкции изображения значительно улучшить его качество, особенно отношение сигнал-шум.
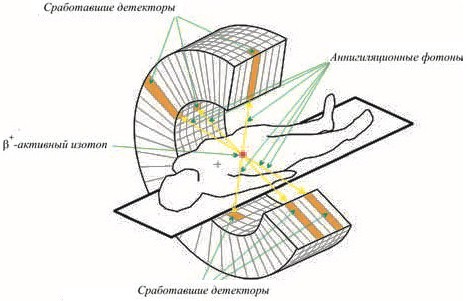
Рис. 6. Схематическое изображение ПЭТ.
В ПЭТ использую радиофармпрепараты содержащие 15 O (период полураспада 2.04 мин),
13 N (9.96 мин). 11 С (20.4 мин). 18 F (110 мин) и др. 18 F обладает оптимальными характеристиками для использования в ПЭТ: наибольшим периодом полураспада и наименьшей энергией β + -излучения. С одной стороны, относительно небольшой период полураспада фтора-18 позволяет получать ПЭТ-изображения высокой контрастности при низкой дозовой нагрузке на пациентов. Низкая энергия позитронного излучения обеспечивает высокое пространственное разрешение ПЭТ-изображений. Относительно большой период полураспада 18 F позволяет располагать его производство отдельно, транспортируя полученный РФП в несколько близлежащих ПЭТ- центров. Наиболее распространенным радиофармпрепаратом (РФП) для ПЭТ является фтордезоксиглюкоза (FDG). Однако, наиболее качественные изображения получаются при использовании таких радионуклидов, как 15 O, 13 N и 11 С
Технология ПЭТ используется для зондирование структуры мозга. Глюкоза наиболее активно поглощается теми областями мозга, которые в данный момент выполняют определенную функцию. ПЭТ позволяют получать изображения областей поглощения маркированной радионуклидом глюкозы. Таким образом выявляются те области мозга, которые связаны с различными видами умственной деятельности.
ПЭТ все чаще используется вместе с КТ или магнитно-резонансной томографией (МРТ). Таким образом практически одновременно получается информация как о структуре, так и о биохимии. ПЭТ наиболее полезна в сочетании с анатомической визуализацией. Современные ПЭТ-сканеры теперь доступны с интегрированными КТ-сканерами, размещенными в одном гантри (ПЭТ-КТ). Два сканирования могут быть выполнены последовательно в течение одного сеанса. Больной не изменяет положение между двумя типами сканирования. Таким образом, функциональная визуализация, получаемая с помощью ПЭТ, который изображает пространственное распределение метаболических или биохимической активности в организме, может быть скоррелировано с анатомической визуализациуй полученной с помощью КТ. ПЭТ-КТ добавляет точность анатомической локализации в функциональную визуализацию, которой ранее не хватало у обычной ПЭТ.
Новые установки ПЭТ состоят почти исключительно из комбинированных сканеров ПЭТ-КТ. Однако, ПЭТ-КТ имеет определенные недостатки, в том числе невозможность одновременно осуществлять сбор данных и значительного дозы облучения пациента, внесенной КТ.
В последнее время активно ведутся работы по альтернативной ПЭТ-КТ гибридной технологии визуализации – технологии ПЭТ-МРТ. По сравнению с КТ МРТ, в частности, дает лучший контраст между мягкими тканями. Вообще, комбинация ПЭТ-МРТ обеспечивает много преимуществ, которые выходят за рамки простого сочетания функциональной информации от ПЭТ с структурной информацией от МРТ. Области клинического применения ПЭТ-МРТ онкология, кардиология и неврология.
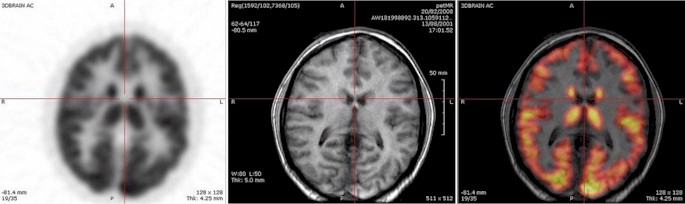
Рис. 7. Снимки экрана компьютера. Слева направо изображения ПЭТ, МРТ и комбинированное изображение ПЭТ-МРТ.
Изотопы для ПЭТ, как правило, вырабатывают на месте проведения исследования. Это связано с тем, что большинство ПЭТ- изотопов являются ультракороткоживущими, с периодами полураспада которые исчисляется несколькими минутами и даже секундами. Ускорители производящие необходимые для ПЭТ часто располагаются вблизи томографа, либо являются составной части комплекса. Поскольку для получения позитронных эмиттеров достаточно иметь протоны с энергией от 10-18 МэВ или дейтроны с энергией 5-9 МэВ (для этой цели подходят малогабаритные циклотроны). Часто томографы поставляются вместе с циклотроном. Кроме того необходима автоматическая радиохимическая лаборатория.
Альтернатива такой организации ПЭТ в ряде случаев − генератор радионуклидов.
Однофотонная эмиссионная компьютерная томография ( ОФЭКТ или, реже, СПЭТ ) - это метод томографической визуализации ядерной медицины с использованием гамма-лучей . [1] Это очень похоже на обычную плоскую визуализацию в ядерной медицине с использованием гамма-камеры (то есть сцинтиграфию ), [2] но способно предоставить истинную трехмерную информацию. Эта информация обычно представлена в виде срезов пациента, но может быть свободно переформатирована или изменена при необходимости.
Этот метод требует доставки пациенту гамма-излучающего радиоизотопа ( радионуклида ), обычно путем инъекции в кровоток. Иногда радиоизотоп представляет собой простой растворимый растворенный ион, такой как изотоп галлия (III). Однако в большинстве случаев радиоизотоп-маркер присоединяется к определенному лиганду для создания радиолиганда , свойства которого связывают его с определенными типами тканей. Этот союз позволяет переносить комбинацию лиганда и радиофармпрепарата и связывать ее с интересующим местом в организме, где концентрация лиганда видна с помощью гамма-камеры.
Содержание

Вместо того, чтобы просто «сфотографировать анатомические структуры», сканирование SPECT отслеживает уровень биологической активности в каждом месте анализируемой трехмерной области. Выбросы радионуклида показывают количество кровотока в капиллярах визуализируемых областей. Точно так же, как обычный рентгеновский снимок представляет собой 2-мерный (2-D) вид трехмерной структуры, изображение, полученное с помощью гамма-камеры, является 2-мерным видом 3-мерного распределения радионуклида .
ОФЭКТ-изображение выполняется с помощью гамма-камеры для получения нескольких двумерных изображений (также называемых проекциями ) под разными углами. Затем используется компьютер для применения алгоритма томографической реконструкции к нескольким проекциям, что дает набор трехмерных данных. Затем этим набором данных можно манипулировать, чтобы показать тонкие срезы вдоль любой выбранной оси тела, аналогичные тем, которые получены с помощью других томографических методов, таких как магнитно-резонансная томография (МРТ), рентгеновская компьютерная томография (рентгеновская КТ) и позитронно-эмиссионная томография (ПЭТ).
ОФЭКТ похожа на ПЭТ в использовании радиоактивного индикаторного материала и обнаружении гамма-лучей. В отличие от ПЭТ, индикаторы, используемые в ОФЭКТ, испускают гамма-излучение, которое измеряется напрямую, тогда как индикаторы ПЭТ испускают позитроны, которые аннигилируют с электронами на расстоянии до нескольких миллиметров, вызывая испускание двух гамма-фотонов в противоположных направлениях. Сканер ПЭТ обнаруживает эти выбросы «совпадающими» во времени, что дает больше информации о локализации событий излучения и, следовательно, изображения с более высоким пространственным разрешением, чем ОФЭКТ (разрешение около 1 см). ОФЭКТ-сканирование значительно дешевле, чем ПЭТ-сканирование, отчасти потому, что оно позволяет использовать более долгоживущие и более легко получаемые радиоизотопы, чем ПЭТ.
Поскольку получение ОФЭКТ очень похоже на получение изображений с помощью планарной гамма-камеры, можно использовать те же радиофармпрепараты . Если пациент обследуется с помощью другого типа сканирования ядерной медицины, но изображения не являются диагностическими, можно перейти прямо к ОФЭКТ, переместив пациента к прибору ОФЭКТ, или даже просто перенастроив камеру для получения изображения ОФЭКТ. пока пациент остается на столе.
Аппарат ОФЭКТ выполняет сканирование костей всего тела. Пациент лежит на столе, который скользит через аппарат, а пара гамма-камер вращается вокруг нее.
Для получения изображений SPECT гамма-камера вращается вокруг пациента. Прогнозы снимаются в определенных точках во время вращения, обычно каждые 3–6 градусов. В большинстве случаев для получения оптимальной реконструкции используется полное вращение на 360 градусов. Время, необходимое для получения каждого прогноза, также варьируется, но обычно составляет 15–20 секунд. Это дает общее время сканирования 15–20 минут.
Гамма-камеры с несколькими головками могут ускорить получение. Например, двухголовая камера может использоваться с головками, разнесенными на 180 градусов друг от друга, что позволяет снимать две проекции одновременно, причем каждая головка требует поворота на 180 градусов. Также используются тройные камеры с шагом 120 градусов.
С помощью ОФЭКТ возможны стробоскопические снимки сердца , а также методы плоской визуализации, такие как сканирование с несколькими стробами (MUGA). Запущенная электрокардиограммой (ЭКГ) для получения дифференциальной информации о сердце в различных частях его цикла, закрытая ОФЭКТ миокарда может использоваться для получения количественной информации о перфузии миокарда, толщине и сократимости миокарда во время различных частей сердечного цикла, а также также для расчета фракции выброса левого желудочка , ударного объема и сердечного выброса.
ОФЭКТ может использоваться в дополнение к любому исследованию гамма-визуализации, где может оказаться полезным истинное трехмерное представление, например, при визуализации опухоли, инфекции ( лейкоцитов ), визуализации щитовидной железы или сцинтиграфии костей .
Поскольку ОФЭКТ обеспечивает точную локализацию в трехмерном пространстве, ее можно использовать для получения информации о локализованных функциях внутренних органов, таких как функциональная визуализация сердца или мозга.
Визуализация перфузии миокарда (MPI) - это форма функциональной визуализации сердца, используемая для диагностики ишемической болезни сердца . Основной принцип заключается в том, что в условиях стресса больной миокард получает меньше кровотока, чем нормальный миокард. MPI - это один из нескольких видов сердечного стресс-теста .
Вводят специфический для сердца радиофармпрепарат, например 99m Tc- тетрофосмин (Myoview, GE healthcare), 99m Tc-сестамиби ( Cardiolite , Bristol-Myers Squibb) или хлорид таллия-201 . После этого частота сердечных сокращений увеличивается, чтобы вызвать миокардиальный стресс, либо упражнениями на беговой дорожке, либо фармакологически аденозином , добутамином или дипиридамолом ( аминофиллин может использоваться для отмены эффектов дипиридамола).
ОФЭКТ-визуализация, выполненная после стресса, показывает распределение радиофармпрепарата и, следовательно, относительный кровоток в различных областях миокарда. Диагностика проводится путем сравнения стрессовых изображений с дополнительным набором изображений, полученных в состоянии покоя, которые обычно получают до стрессовых изображений.
Было продемонстрировано, что общая точность MPI составляет около 83% ( чувствительность : 85%; специфичность : 72%) (в обзоре, не только для SPECT MPI), [3] и сопоставима (или лучше) с другими не -инвазивные тесты на ишемическую болезнь сердца.
Обычно гамма-излучающий индикатор, используемый при функциональной визуализации мозга, представляет собой экзаметазим технеция (99mTc) . 99m Tc - это метастабильный ядерный изомер , излучающий гамма-лучи, обнаруживаемые с помощью гамма-камеры. Присоединение его к экзаметазиму позволяет ему поглощаться тканями мозга пропорционально мозговому кровотоку, что, в свою очередь, позволяет оценить церебральный кровоток с помощью ядерной гамма-камеры.
Поскольку кровоток в головном мозге тесно связан с локальным метаболизмом мозга и потреблением энергии, индикатор 99m Tc-экзаметазим (а также аналогичный индикатор 99m Tc-EC) используется для региональной оценки метаболизма мозга в попытке диагностировать и дифференцировать различные причинные патологии деменции . Метаанализ многих опубликованных исследований показывает, что чувствительность ОФЭКТ с этим индикатором составляет около 74% при диагностике болезни Альцгеймера по сравнению с чувствительностью 81% при клиническом обследовании ( когнитивные тесты и т. Д.). Более поздние исследования показали, что точность ОФЭКТ в диагностике болезни Альцгеймера может достигать 88%. [4] В метаанализе ОФЭКТ превзошла клиническое обследование и клинические критерии (91% против 70%) в способности дифференцировать болезнь Альцгеймера от сосудистой деменции. [5] Эта последняя способность связана с визуализацией локального метаболизма головного мозга с помощью ОФЭКТ, при которой точечная потеря коркового метаболизма, наблюдаемая при множественных инсультах, явно отличается от более равномерной или «плавной» потери не затылочной корковой функции мозга, типичной для болезни Альцгеймера. болезнь. Другая недавняя обзорная статья показала, что многоголовые ОФЭКТ-камеры с количественным анализом дают общую чувствительность 84-89% и общую специфичность 83-89% в поперечных исследованиях, чувствительность 82-96% и специфичность 83-89 % для продольных исследований деменции. [6]
ОФЭКТ-сканирование 99m Tc-экзаметазимом конкурирует с ПЭТ- сканированием на основе флудезоксиглюкозы (ФДГ) головного мозга, которое позволяет оценить региональный метаболизм глюкозы в головном мозге, чтобы получить очень похожую информацию о локальном повреждении мозга в результате многих процессов. ОФЭКТ более широко доступна, потому что используемый радиоизотоп более долговечен и намного дешевле в ОФЭКТ, а также менее дорогое оборудование для гамма-сканирования. В то время как 99m Tc извлекается из относительно простых генераторов технеция-99m , которые еженедельно доставляются в больницы и сканирующие центры для получения свежего радиоизотопа, FDG PET полагается на FDG, который производится на дорогостоящем медицинском циклотроне. и «горячая лаборатория» (автоматизированная химическая лаборатория для производства радиофармпрепаратов), а затем немедленно доставляется в места сканирования из-за естественного короткого периода полураспада фтора-18 - 110 минут .
В ядерной энергетике метод SPECT может быть применен для визуализации распределения радиоизотопов в облученном ядерном топливе. [7] Из-за облучения ядерного топлива (например, урана) нейтронами в ядерном реакторе, в топливе естественным образом образуется широкий спектр гамма-излучающих радионуклидов, таких как продукты деления ( цезий-137 , барий-140 и европий). -154 ) и продуктов активации ( хром-51 и кобальт-58 ). Их можно отобразить с помощью ОФЭКТ, чтобы проверить наличие топливных стержней в хранимой топливной сборке для целей гарантий МАГАТЭ [8], чтобы подтвердить предсказания кодов моделирования активной зоны, [9] или изучить поведение ядерного топлива при нормальной работе [10] или в аварийных сценариях. [11]

Восстановленные изображения обычно имеют разрешение 64 × 64 или 128 × 128 пикселей с размерами пикселей в диапазоне 3–6 мм. Количество получаемых проекций выбирается приблизительно равным ширине получаемых изображений. Как правило, полученные восстановленные изображения будут иметь более низкое разрешение, будут иметь повышенный шум, чем плоские изображения, и будут подвержены артефактам .
Сканирование занимает много времени, и важно, чтобы во время сканирования пациент не двигался. Движение может вызвать значительное ухудшение восстановленных изображений, хотя методы восстановления с компенсацией движения могут помочь в этом. Крайне неравномерное распределение радиофармпрепарата также может вызвать артефакты. Область очень интенсивной активности (например, мочевой пузырь) может вызвать появление обширных полос на изображениях и затемнить соседние области активности. Это ограничение алгоритма реконструкции отфильтрованной обратной проекции . Итерационная реконструкция - это альтернативный алгоритм, значение которого становится все более важным, поскольку он менее чувствителен к артефактам и может также корректировать затухание и размытие, зависящее от глубины. Кроме того, итерационные алгоритмы могут быть сделаны более эффективным использованием Superiorization методологии. [12]
Рассеяние гамма-лучей, а также случайный характер гамма-лучей также могут привести к ухудшению качества изображений SPECT и вызвать потерю разрешения. Для улучшения разрешения изображений SPECT также применяются коррекция рассеяния и восстановление разрешения. [13]
В некоторых случаях гамма-сканер SPECT может быть построен для работы с обычным компьютерным томографом с одновременной регистрацией изображений. Как и при ПЭТ / КТ , это позволяет определять местонахождение опухолей или тканей, которые можно увидеть на сцинтиграфии ОФЭКТ, но которые трудно точно определить относительно других анатомических структур. Такое сканирование наиболее полезно для тканей за пределами мозга, где расположение тканей может быть гораздо более разнообразным. Например, ОФЭКТ / КТ может использоваться в приложениях сканирования паращитовидных желез сестамиби , где этот метод полезен при обнаружении эктопических аденом паращитовидных желез, которые могут находиться не на своих обычных местах в щитовидной железе. [14]
Общая производительность систем SPECT может быть выполнена с помощью инструментов контроля качества, таких как фантом Ящака . [15]
Однофотонная эмиссионная компьютерная томография ( ОФЭКТ или, реже, СПЭТ ) - это метод томографической визуализации ядерной медицины с использованием гамма-лучей . [1] Это очень похоже на обычную плоскую визуализацию в ядерной медицине с использованием гамма-камеры (то есть сцинтиграфию ) [2], но может предоставить истинную трехмерную информацию. Эта информация обычно представлена в виде срезов пациента, но при необходимости ее можно свободно переформатировать или изменять.
Этот метод требует доставки пациенту гамма-излучающего радиоизотопа ( радионуклида ), обычно путем инъекции в кровоток. Иногда радиоизотоп представляет собой простой растворимый растворенный ион, такой как изотоп галлия (III). Однако в большинстве случаев радиоизотоп-маркер присоединяется к определенному лиганду для создания радиолиганда , свойства которого связывают его с определенными типами тканей. Это сочетание позволяет переносить комбинацию лиганда и радиофармпрепарата и связывать ее с интересующим местом в организме, где концентрация лиганда видна с помощью гамма-камеры.
Читайте также:




