Таблица сравнение процессоров фаго и пиноцитоза
Конкурс «Био/Мол/Текст»-2021/2022
Эта работа опубликована в номинации «Школьная» конкурса «Био/Мол/Текст»-2021/2022.
Партнер номинации — некоммерческая школа-пансион «Летово».
Генеральный партнер конкурса — международная инновационная биотехнологическая компания BIOCAD.
Генеральный партнер конкурса — компания «Диаэм»: крупнейший поставщик оборудования, реагентов и расходных материалов для биологических исследований и производств.
Микроглия и заболевания
Болезнь Альцгеймера
Болезнь Альцгеймера — самое распространенное нейродегенеративное заболевание, одна из важнейших причин смертности людей во всем мире. Болезнь Альцгеймера чаще всего возникает у людей старше 50 лет и характеризуется прогрессивным снижением интеллекта, нарушением памяти и изменением личности.
По одной из гипотез, причиной возникновения заболевания является накопление бета-амилоидов (пептиды, состоящие примерно из 40 аминокислотных остатков) и их отложение в бляшках.
На ранних стадиях развития болезни микроглия замедляет токсическое действие бета-амилоида, образуя защитный барьер вокруг него и замедляя повреждающее действие амилоида (рис. 4) [8].
Но позже микроглия не только перестает выполнять защитную функцию, а еще и становится причиной обострения болезни (рис. 4) [8].

Рисунок 4. Левая сторона картинки (1–4) иллюстрирует защитное действие микроглии.
1 — очищение микроглией Aβ посредством макропиноцитоза;
2 — поглощение микроглией липопротеин-ассоциированного Aβ;
3 — фагоцитоз фибриллярных агрегатов Aβ;
4 — формирование больших отложений в бляшки.
Правая сторона (5–7) — действие микроглии, обостряющее БА.
5 — Аβ-фибриллы на краях бляшек, созданных микроглией, действуют как субстрат для новой Aβ-фибрилляции;
6 — секреция микроглией цитокинов, которые активируют астроциты;
7 — разрушение синапсов.
Дело в том, что белок C1q (белок, экспрессирующийся в мозге, уровень которого сильно повышается с возрастом, особенно в гиппокампе) при связывании с Aβ может вызвать активацию классического каскада комплемента, то есть активировать микроглию к разрушению синапсов [8].
К тому же микроглия усугубляет тау-патологию (возникающие в нейронах при болезни Альцгеймера агрегаты тау-белка), реагируя на умирающие нейроны и белковые агрегаты высвобождением цитокинов. Цитокины — медиаторы воспаления, активируют астроциты, способствуя этим уничтожению нейронов [8].
Из этого можно сделать вывод, что на поздних стадиях заболевания микроглия, разрушая синапсы, усугубляя патологию тау и вырабатывая медиаторы воспаления, является одной из причин снижения когнитивных функций, и поэтому возможно истощение микроглии и блокировка путей, активирующих систему фагоцитоза, могут улучшать состояние пациентов при болезни Альцгеймера.
Развитие и функции микроглии
Развитие микроглии

Рисунок 2. Схема происхождения клеток крови и лимфы из гемопоэтической стволовой клетки.
Микроглия похожа на периферические моноциты и макрофаги (рис. 2) — клетки иммунной системы, которые производит красный костный мозг, и раньше считалось, что она происходит от циркулирующих моноцитов [2]. Но на сегодняшний день доказано, что микроглия формируется гораздо раньше и имеет немного отличное от периферических клеток происхождение. Она возникает из примитивных макрофагов эмбрионального желточного мешка [2]. Эти клетки появляются так рано, что попадают в мозг через кровеносную систему, раньше образования гематоэнцефалического барьера (рис. 3) [2].

Рисунок 3. Клетки микроглии образуются из примитивных макрофагов, которые выделяются из эмбрионального желточного мешка во время развития (до 8,5 дня эмбриона) и попадают в зачатки мозга через систему кровообращения до появления гематоэнцефалического барьера. На 9,5 день эмбриона они окружают нейроэпителий и через день попадают туда, начиная колонизировать паренхиму центральной нервной системы.
Фагоцитирующие клетки. Фагоциты. Полиморфно-ядерные лейкоциты ( гранулоциты ). Нейтрофилы. Феномен краевого стояния. Нейтрофилия. Эозинофилия.
Фагоциты выполняют не только защитные (поглощают и разрушают чужеродные агенты), но и дренажные функции (удаляют погибшие и деградировавшие структуры организма). Фагоциты представлены клетками миелопоэтического ряда (полиморфно-ядерные лейкоциты) и макрофагально-моноцитарной системы (моноциты, тканевые макрофаги). Основные свойства фагоцитирующих клеток представлены в табл. 10-5.
Полиморфно-ядерные лейкоциты имеют дольчатое ядро и множество мелких цитоплаз-матических гранул (поэтому их также называют гранулоциты). По окрашиванию гранул выделяют три типа клеток: нейтрофилы, эозинофилы и базофилы.
Таблица 10-5. Характеристики фагоцитирующих клеток
| Клетки | Источник | Формы участия в защитных реакциях |
| Нейтрофилы | Костный мозг; после дифференцировки выходят в кровоток | Адгезия к эндотелию и выход за пределы кровотока; хемотаксис; поглощение; дегрануляция; секреция О 2 -зависимых и О 2 -независимых микробицидных факторов |
| Эозинофилы | Тот же | Секреция О2-зависимых и 02-независимых микробицидных факторов, направленных против паразитов (простейшие и гельминты) |
| Моноциты | Костный мозг; после дифференцировки промоноциты выходят в кровоток | Адгезия к эндотелию и выход за пределы кровотока; хемотаксис; поглощение; дегрануляция; секреция О2-зависимых и О2-независимых микробицидных факторов (включая цитокины) |
| Макрофаги (клетки фон Купффера, альвеолярные макрофаги, гистиоциты, перитонеальные макрофаги, клетки мик-роглии, макрофаги селезёнки и др.) | Моноциты периферической крови | Адгезия к эндотелию и выход за пределы кровотока; хемотаксис; поглощение; дегрануля-ция; секреция О2-зависимых и О2-независимых микробицидных факторов; синтез компонентов комплемента, активатора ппазминогена и других протеаз; секреция медиаторов и компонентов клеточных мембран, включая продукты I и II классов МНС; участие в иммунных реакциях |
Гомеостатические функции
Во время раннего развития мозга микроглия может высвобождать нейротрофические факторы, тем самым влияя на формирование, выживание и дифференцировку нейронов, создание нейронных сетей. Например, во время развития мозга она устраняет дефектные нейроны, не подвергшиеся апоптозу [2].
Апоптоз — процесс программируемой клеточной гибели, в результате которого клетка распадается на отдельные апоптотические тельца, ограниченные плазматической мембраной. Подробнее читайте в статье «Апоптоз или Путь самурая» [6].
Реактивация иммунного ответа — актуальное направление антираковой терапии
Таким образом, в ближайшем окружении опухолей присутствует сложная смесь молекул: как активирующих, так и ингибирующих иммунный ответ. Перспективы развития опухоли (а значит, перспективы выживания организма) зависят от баланса ингредиентов этого «коктейля». Если будут преобладать иммуноактиваторы — значит, опухоль не справилась с задачей и будет уничтожена или ее рост сильно затормозится. Если же преобладают иммуносупрессорные молекулы — это значит, что опухоль смогла подобрать ключ и начнет быстро прогрессировать. Понимая механизмы, которые позволяют опухолям подавлять наш иммунитет, мы сможем разработать контрмеры и сдвинуть баланс в сторону уничтожения опухолей [8].
Как показывают эксперименты, «перепрограммирование» макрофагов (и других клеток иммунной системы) обратимо. Поэтому одним из перспективных направлений онко-иммунологии на сегодняшний день является идея «реактивации» собственных клеток иммунной системы пациента с целью усиления эффективности других методов лечения. Для некоторых разновидностей опухолей (например, меланом) это позволяет добиться впечатляющих результатов. Другой пример, обнаруженный группой Меджитова [9], — обычный лактат, молекула, которая производится при недостатке кислорода в быстрорастущих опухолях за счет эффекта Варбурга [10]. Эта простая молекула стимулирует перепрограммирование макрофагов, заставляя их поддерживать рост опухоли. Лактат транспортируется внутрь макрофагов через мембранные каналы, и потенциальная терапия заключается в блокировке этих каналов.
Развитие методов антираковой терапии в настоящее время идет по нескольким направлениям сразу , и все они важны. Ведь научившись управлять иммунным ответом так же эффективно, как это делают злокачественные опухоли, мы сумеем окончательно «переиграть» эту болезнь, которая остается одной из главных причин смертности в России и в мире.
Биомаркеры [11] и биоинформатический анализ [12] — лишь некоторые из таких методов. — Ред.

Обзор
Микроглия.
Автор
Редакторы
Статья на конкурс «Био/Мол/Текст»: Микроглия — клетки, возникающие из примитивных макрофагов. Они развиваются в эмбриональном желточном мешке, затем попадают в мозг, через систему кровообращения.
Микроглия способствует выживанию и гибели нейронов, а также может обрезать синаптические связи, способствуя формированию функционирующих зрелых нервных цепей. Этот процесс напрямую связан с памятью.
Микроглия имеет большое значение при нейродегенеративных заболеваниях, таких как болезнь Альцгеймера и паркинсонизм.
В этой статье я постаралась рассказать о том, что такое микроглия и как она участвует в сложных процессах формирования памяти, забывания и в развитии заболеваний.

Функции микроглии
Клетки микроглии выполняют иммунную функцию. Они подвижны — умеют ползать как амебы — и способны реагировать на широкий спектр проблем, таких как гибель дофаминергических нейронов при паркинсонизме или даже на бактериальные и паразитарные инфекции. При обнаружении специфического фактора микроглиальные клетки быстро «подстраиваются» под проблему, меняя свою морфологию, фенотип и функции. Это наблюдается при нейродегенеративных заболеваниях, инфекциях, опухолях, черепно-мозговых травмах и т. п. [2].
Например, при рассеянном склерозе микроглия активируется с помощью цитокинов и костимулирующих молекул, после чего у нее появляется способность реактивировать лимфоциты, способствуя этим уничтожению дегенерирующих нейронов [4].
Но кроме иммунной функции, микроглия напрямую связана с развитием мозга, памятью и обучением [5].
Нейтрофилы. Феномен краевого стояния. Нейтрофилия. Эозинофилия
Нейтрофилы — основные эффекторные клетки острого воспаления; у взрослых лиц они составляют самую многочисленную популяцию лейкоцитов. Основная часть нейтрофилов циркулирует в крови в течение 6-7 ч. Затем они скапливаются в капиллярах, где формируют краевой пул, прикрепляясь к эндотелию (по периметру кровотока); в таком состоянии нейтрофилы находятся в готовности немедленно покинуть кровеносное русло (феномен краевого стояния). Нейтрофилия (увеличение их количества в периферической крови) часто указывает на наличие воспалительной реакции.
Потенциал эозинофилов направлен не столько на фагоцитирование бактерий, сколько на нейтрализацию паразитов, особенно гельминтов (например, нематод). Поэтому, эозинофилия — признак, указывающий на возможную глистную инвазию. Кроме того, эозинофилы участвуют в разрушении гистамина, выделяя гистаминазу. Именно поэтому эозинофилию также наблюдают при аллергических заболеваниях. Определённая роль в подобной специализации эозинофилов принадлежит специфическим гранулам, содержащим пероксидазы и катионные белки (например, основный белок, катионные белки эозинофилов), активные именно в отношении паразитов. В активации эозинофилов важную роль играют IgE, образующиеся в ответ на сенсибилизацию организма аллергенами (в том числе микробными).
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Конкурс «био/мол/текст»-2014
Эта статья представлена на конкурс научно-популярных работ «био/мол/текст»-2014 в номинации «Лучший обзор».

Главный спонсор конкурса — дальновидная компания Генотек.
Конкурс поддержан ОАО «РВК».
Спонсором номинации «Биоинформатика» является Институт биоинформатики.
Спонсором приза зрительских симпатий выступила фирма Helicon.
Свой приз также вручает Фонд поддержки передовых биотехнологий.
Видео стадии фагоцитоза и питание клетки
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021

Обзор
Макрофаг атакует раковую клетку
Автор
Редакторы
Статья на конкурс «био/мол/текст»: Иммунная система — это мощная многослойная защита нашего организма, которая потрясающе эффективна против вирусов, бактерий, грибов и других патогенов извне. Кроме того, иммунитет способен эффективно распознавать и уничтожать трансформированные собственные клетки, которые могут перерождаться в злокачественные опухоли. Однако сбои в работе иммунной системы (по генетическим либо другим причинам) приводят к тому, что однажды злокачественные клетки берут верх. Разросшаяся опухоль становится нечувствительной к атакам организма и не только успешно избегает уничтожения, но и активно «перепрограммирует» защитные клетки для обеспечения собственных нужд. Поняв механизмы, которые опухоль использует для подавления иммунного ответа, мы сможем разработать контрмеры и попытаться сдвинуть баланс в сторону активации собственных защитных сил организма для борьбы с болезнью.

Болезнь Паркинсона
Болезнь Паркинсона (БП) — это нейродегенеративное заболевание, при котором нейроны накапливают включения α-синуклеина (чаще всего их называют тельцами Леви), а дофаминергические нейроны черной субстанции погибают.
Как и при болезни Альцгеймера, на ранних стадиях болезни Паркинсона микроглия замедляет прогрессирование болезни, так как, разрушая α-syn, она помогает избавиться от его избытка. Эта мысль подтверждается многими исследованиями (было показано, что при препятствии очищению микроглией α-синуклеина увеличивается продукция противовоспалительных цитокинов, что способствует гибели нейронов и двигательной дисфункции) [9].
На последующих стадиях заболевания микроглия уничтожает дегенерирующие нейроны, однако «доброе» ли это дело или «злое» в контексте работы нервной системы и патогенеза болезни, сказать сложно.
Макрофаги — «клетки-воины» и «клетки-целители»
Макрофаги, пожалуй, самые знаменитые клетки врожденного иммунитета — именно с изучения их способностей к фагоцитозу Мечниковым и началась классическая клеточная иммунология. В организме млекопитающих макрофаги — боевой авангард: первыми обнаруживая врага, они не только пытаются уничтожить его собственными силами, но также привлекают к месту сражения другие клетки иммунной системы, активируя их. А после уничтожения чужеродных агентов принимаются активно участвовать в ликвидации причиненных повреждений, вырабатывая факторы, способствующие заживлению ран. Эту двойственную природу макрофагов опухоли используют себе на пользу.
В зависимости от преобладающей активности различают две группы макрофагов: М1 и М2. М1-макрофаги (их еще называют классически активированными макрофагами) — «воины» — отвечают за уничтожение чужеродных агентов (в том числе и опухолевых клеток), как напрямую, так и за счет привлечения и активации других клеток иммунной системы (например, Т-киллеров). М2 макрофаги — «целители» — ускоряют регенерацию тканей и обеспечивают заживление ран [4], [8].
Присутствие в опухоли большого количества М1-макрофагов тормозит ее рост [5], а в некоторых случаях может вызвать даже практически полную ремиссию (уничтожение). И наоборот: М2-макрофаги выделяют молекулы — факторы роста, которые дополнительно стимулируют деление опухолевых клеток, то есть благоприятствуют развитию злокачественного образования. Экспериментально было показано, что в опухолевом окружении обычно преобладают именно М2-клетки («целители»). Хуже того: под действием веществ, выделяемых опухолевыми клетками, активные М1-макрофаги «перепрограммируются» в М2-тип [6], перестают синтезировать антиопухолевые цитокины, такие как интерлейкин-12 (IL12) или фактор некроза опухолей (TNF) и начинают выделять в окружающую среду молекулы, ускоряющие рост опухоли и прорастание кровеносных сосудов, которые будут обеспечивать ее питание, например фактор роста опухолей (TGFb) и фактор роста сосудов (VGF). Они перестают привлекать и инициировать другие клетки иммунной системы и начинают блокировать местный (противоопухолевый) иммунный ответ (рис. 2).
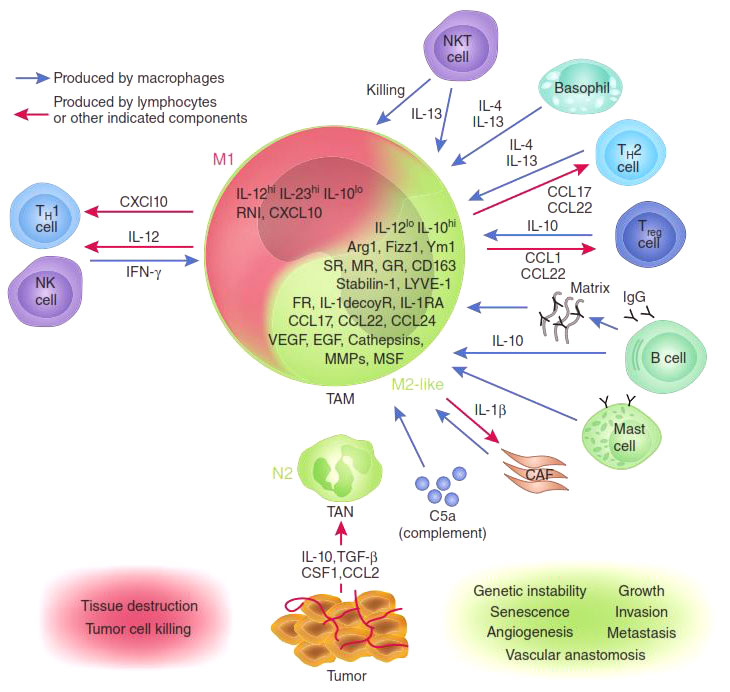
Рисунок 2. М1- и М2-макрофаги: их взаимодействие с опухолью и другими клетками иммунной системы.
Ключевую роль в этом перепрограммировании играют белки семейства NF-kB [7]. Эти белки являются транскрипционными факторами, контролирующими активность множества генов, необходимых для М1 активации макрофагов. Наиболее важные представители этого семейства — р65 и р50, вместе образующие гетеродимер р65/р50, который в макрофагах активирует множество генов, связанных с острым воспалительным ответом, таких как TNF, многие интерлейкины, хемокины и цитокины. Экспрессия этих генов привлекает все новые и новые иммунные клетки, «подсвечивая» для них район воспаления. В то же время другой гомодимер семейства NF-kB — р50/р50 — обладает противоположной активностью: связываясь с теми же самыми промоторами, он блокирует их экспрессию, снижая градус воспаления.
И та, и другая активность NF-kB транскрипционных факторов очень важна, но еще важнее равновесие между ними. Было показано, что опухоли целенаправленно выделяют вещества, которые нарушают синтез p65 белка в макрофагах и стимулируют накопление ингибиторного комплекса р50/р50 [7]. Таким способом (помимо еще ряда других) опухоль превращает агрессивных М1-макрофагов в невольных пособников своего собственного развития: М2-тип макрофагов, воспринимая опухоль как поврежденный участок ткани, включают программу восстановления, однако секретируемые ими факторы роста только добавляют ресурсы для роста опухоли. На этом цикл замыкается — растущая опухоль привлекает новые макрофаги, которые перепрограммируются и стимулируют ее рост вместо уничтожения.
Синаптическая пластичность, память и обучение
Формирование памяти — это процесс, в основе которого лежит физиологическое явление, называемое долговременной потенциацией. При долговременной потенциации проведение нервного импульса между нейронами приводит к резкому усилению проведения последующих импульсов в образованном ими синапсе. Это происходит из-за того, что долговременная потенциация упрочняет связи между нейронами и ускоряет проведение нервного импульса по цепочкам нейронов, которые уже передавали информацию [7].
Сила синапса — это сила сигнала, который он посылает в клетку-мишень, а синаптическая пластичность — возможность изменения силы синапса.
Силу синапса регулируют не только сами нейроны, но и микроглия, которая, помимо «ненужных» нейронов, может разрушать синаптические связи, тем самым контролируя синаптическую активность и пластичность [5].
Эта функция микроглии крайне важна для правильного развития мозга и влияет на активность нейронов, так как клетки выборочно обрезают избыточные нейрональные процессы, которые могут мешать формированию зрелых, функционирующих нейронных сетей.
Введение
Глия, или нейроглия — это разнофункциональные клетки нервной ткани, формирующие специфическое микроокружение для нейронов. Они обеспечивают условия для их выживания и работы.

Рисунок 1. Нейроглия. Бледно-розовые клетки — эпендимоциты, голубые — олигодендроциты, зеленые — астроциты, а темно-красные — клетки микроглии. Также на картинке присутствуют кровеносные сосуды (красные) и нейроны (желтые).
Самая распространенная группа нейроглии — олигодендроциты (рис. 1). Олигодендроциты создают изолирующее покрытие вокруг аксона, которое называется миелиновым. Оно нужно для высокой скорости проведения сигналов [1].
Еще есть астроциты (рис. 1); их основной функцией является создание гематоэнцефалического барьера, который защищает нервную систему от вредных веществ, способных проникнуть через кровь. А также эпендимные клетки (рис. 1), некоторые из которых тоже участвуют в образовании гематоэнцефалического барьера, а другие выполняют секреторную функцию или передают информацию о составе цереброспинальной жидкости на капиллярную сеть. Также эпендимная глия — источник стволовых нервных клеток.
Эти три группы объединяют в макроглию, но помимо нее существует еще микроглия, о которой я и хочу рассказать в своей статье.
В последнее время количество работ, посвященных исследованию микроглии, сильно возросло. Изучаются не просто ее иммунные функции, но также влияние на память, обучение и участие в нейродегенеративных заболеваниях. История про маленькие клетки в мозге, которые «съедают» неповторяемые нами стихотворения, сама по себе интересна, а если эти клетки еще и «плохие» нейроны уничтожают — тем более.
Дуализм иммунного ответа и его значение в канцерогенезе
Существует множество научных статей, описывающих, как иммунная система борется с опухолевыми клетками, но не меньшее количество публикаций демонстрирует, что присутствие клеток иммунной системы в ближайшем опухолевом окружении является негативным фактором, коррелирующим с ускоренным ростом и метастазированием рака [2], [3]. В рамках концепции иммуноредактирования, описывающей, как изменяется характер иммунного ответа по мере развития опухоли, подобное двойственное поведение наших защитников получило, наконец, свое объяснение.
Мы рассмотрим некоторые механизмы того, как это происходит, на примере макрофагов. Похожие приемы опухоль использует и для того, чтобы обманывать другие клетки врожденного и приобретенного иммунитета.
Распределение микроглии
Микроглия распределяется неравномерно. Ее распределение может зависеть от областей мозга — и даже модулироваться половыми гормонами [3].
Региональные различия связаны с разной экспрессией генов. Например, в желудочковой/субвентрикулярной зоне базальными предшественниками (клетки-предшественники внутренних слоев субвентрикулярной зоны с неполярной морфологией) секретируется определенный ген (CXCL12). Именно CXCL12 влияет на привлечение микроглии в эти зоны. Уменьшение количества базальных предшественников уменьшает и количество микроглии, в то время как оно, в свою очередь, влияет на количество нейрональных предшественников в этих же зонах. И из-за того, что микроглия контролирует убиквитин‐специфическую протеазу 18, которая в здоровых условиях уменьшает разрушение тканей, в этой зоне ткани разрушаются чаще, чем в остальных [3].
Механизм и пути эндоцитоза белков в клетке
• Для захвата материала из окружающей среды клетка использует несколько различных механизмов
• В последующих превращениях захваченного материала важную роль играют ферменты деградации и низкое значение pH в эндосомах и лизосомах
Эндоцитоз — процесс, при котором эукариотическая клетка захватывает материал из окружающей среды при образовании везикул на плазматической мембране. Во многом являясь противоположностью экзоцитоза, эндоцитоз обладает несколькими функциями:
• поглощение питательных веществ;
• регуляция экспрессии белков на клеточной поверхности, например рецепторов гормонов и переносчиков глюкозы, что дает возможность клетке контролировать процесс захвата лигандов;
• захват и деградация внеклеточного дебриса;
• восстановление мембраны, встроенной в плазматическую мембрану при секреции.
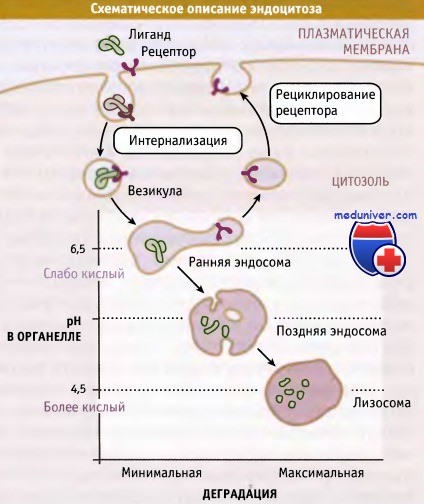
Среди органелл, участвующих в эндоцитозе, существует градиент pH и активности ферментов деградации.
При эндоцитозе макромолекулы или рециклируют в плазматическую мембрану, или разрушаются.
Наряду с этим, процесс эндоцитоза используется для проникновения в клетку патогенными организмами, такими как бактерии, простейшие и вирусы.
При эндоцитозе образующиеся на плазматической мембране везикулы сливаются с органеллами. Эти органеллы обладают двумя важными особенностями: в люмене у них поддерживается кислая среда, и находятся протеолитические ферменты, оптимальная активность которых проявляется при кислых значениях pH.
Органеллы характеризуются различной степенью кислотности среды и различным содержанием ферментов деградации. Они подразделяются на ранние и поздние эндосомы и лизосомы, которые обладают широким спектром протеолитической активности соответственно от минимального в эндосомах до максимального в лизосомах.
В лизосомах находятся ферменты деградации, активные по отношению практически ко всем биополимерам (белкам, липидам, углеводам, РНК, ДНК), попадающим в них путем эндоцитоза. Хотя в течение долгого времени лизосомы рассматривались как терминальные органеллы на пути эндоцитоза, существуют данные о том, что они иногда могут сливаться с плазматической мембраной.
Протонный насос, функционирующий за счет энергии АТФ, называется вакуолярной АТФазой (v-АТФаза) и переносит ионы Н+ из цитозоля в люмен определенных органелл. При этом pH внутри органелл, по сравнению с цитозолем, уменьшается. Значение pH цитозоля составляет 7,4. Внутри ранних эндосом поддерживается слегка кислое значение pH (6,5-6,8), а в поздних эндосомах и в лизосомах значение pH достигает 4,5.
Величина pH в различных эндосомальных компартментах регулируется разными факторами, такими как содержание и активность v-АТФазы, а также ионной проводимостью и свойствами других транспортных АТФаз, присутствующих в мембранах различных эндосом. Важно отметить, что pH в каждом компартменте зависит от выполняемой им функции.
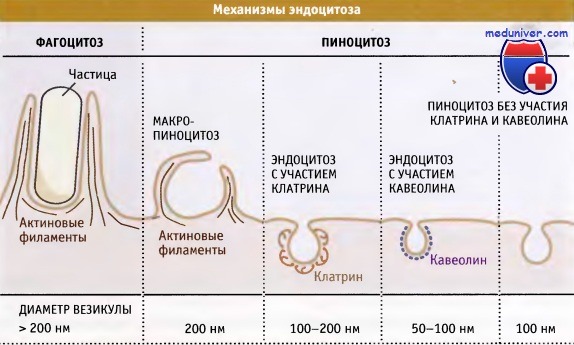
Существует несколько механизмов эндоцитоза.
Исторически сложилось так, что эндоцитоз стали подразделять на фагоцитоз («поедание клеткой») и пиноцитоз («впитывание клеткой»), что отражает объем попадающего в клетку материала. Специализированный фагоцит, например макрофаг, может заключать материал в везикулу, диаметром до 10 мкм. Сходство с процессом поглощения пищи подчеркивается также сильно кислой внутренней средой фагосом, оптимальной для активности ферментов, расщепляющих поглощенные белки, липиды и углеводы.
Почти все клетки обладают способностью к фагоцитозу, однако этот процесс наиболее характерен для специализированных клеток иммунной системы, таких как макрофаги и дендритные клетки, поглощающих патогенные микроорганизмы и помогающих формировать ся защитной реакции у организма хозяина. Макрофаги также участвуют в очистке организма от стареющих или апоптотических клеток путем фагоцитоза, происходящего даже в отсутствие инфекции. Поскольку настоящие фагоциты обладают специфическими рецепторами, запускающими фагоцитоз, они более эффективны в захвате частиц по сравнению с другими клетками. Например, макрофаги и некоторые другие фагоцитирующие клетки экспрессируют рецепторы для молекул антител.
Пиноцитоз представляет собой общий термин, включающий несколько механизмов захвата. Обычно при этом образуется небольшая эндоцитозная везикула, достигающая 0,1-0,3 мкм в диаметре. Наиболее полно изученной разновидностью пиноцитоза является эндоцитоз, опосредуемый рецепторами. В ранних исследованиях по захвату липопротеинов низкой плотности (ЛНП) соответствующими рецепторами было получено много концептуальных сведений, способствующих нашему пониманию механизмов эндоцитоза. Большое количество рецепторов, расположенных на поверхности клеток, связывает лиганды, к числу которых относятся питательные вещества, ростовые факторы, гормоны, антитела или антигены.
Комплексы «рецептор-лиганд» поглощаются, накапливаясь в специфических областях плазматической мембраны, которые называются «окаймленные ямки». Окаймленные ямки отпочковываются, образуя везикулы, которые сливаются с ранними эндосомами. В кислой среде внутри эндосом связь некоторых лигандов с рецепторами разрывается, причем рецепторы направляются назад, на поверхность клетки, а лиганды — в поздние эндосомы и потом в лизосомы. Некоторые комплексы рецептора и лиганда в ранних эндосомах не диссоциируют, а вместо этого, так же как свободные лиганды, направляются в лизосомы.
Существует несколько вариантов основного пути эндоцитоза. Некоторые клетки содержат лизосомы, в которых происходит лишь частичная деградация поглощенного материала, что существенно для выработки иммунного ответа на захваченные патогены. Хорошим примером являются дендритные клетки, представляющие собой клетки лейкоцитарного происхождения, присутствующие в крови и во всех тканях организма.
Они инициируют почти все иммунные реакции, что обусловлено их уникальной способностью стимулировать В- и Т-лимфоциты, узнающие и уничтожающие патогены. Дендритные клетки захватывают циркулирующие антигены или патогенные микроорганизмы и доставляют их в специальный компартмент лизосом. Эти лизосомы не обладают способностью к полному перевариванию белков, что благоприятствует образованию коротких пептидов (10-15 остатков аминокислот), связывающихся с белками главного комплекса гистосовместимости класса II (МНС). Еще одна особенность этих лизосом позволяет комплексам пептидов и МНС класса II выходить из них за счет образования длинных трубочек, по которым содержимое транспортируется к плазматической мембране. Затем комплексы пептида и МНС класса II выходят на поверхность мембраны, где они стимулируют эффекторные клетки.

Электронная микрофотография макрофага,
поглощающего эритроцит.
Еще один вариант эндоцитоза предполагает, что поглощенный клеткой материал полностью минует лизосомный путь. Этот процесс носит название трансцитоз, он характерен для специализированных эпителиальных клеток, выстилающих полости тела, например внутреннюю поверхность кишечника.
Функция эпителиальных клеток состоит в регуляции транспорта материалов между организмом и окружающей средой. Эти клетки тесно примыкают друг к другу и образуют непрерывный слой. Они поляризованы, причем «апикальная» поверхность обращена в сторону люмена кишки, а «базальная» — в противоположную сторону, к крови. Обычно трансцитоз начинается с образования покрытой клатрином везикулы на апикальной или базолатеральной мембране. Эта везикула сливается с ранней эндосомой, что приводит к образованию трансцитозной везикулы, принадлежащей к типу рециклирующих везикул. Трансцитозная везикула переносится на противоположную поверхность клетки и сливается с мембраной.
При всасывании в кишечнике питательных веществ некоторые транспортные везикулы, которые образуются при эндоцитозе на апикальной поверхности, продвигаются прямо на базальную сторону и таким образом доставляют интернализированные компоненты без риска их разрушения в лизосомах. Еще одним примером трансцитоза является перенос факторов гуморального иммунитета от матери к новорожденному. Иммуноглобулины, присутствующие в материнском молоке, в кишечнике ребенка захватываются апикальными рецепторами, которые транспортируют их на другую сторону эпителия и доставляют в плазму крови.
Наряду с переносом через окаймленные ямки, на плазматической мембране образуются другие типы эндоцитозных везикул. Кавеолы представляют собой небольшие инвагинации в поверхности мембран, покрытые кавеолином. По-видимому, в кавеолах накапливаются некоторые рецепторы и мембранные липиды, которые не переносятся через окаймленные ямки. Эти рецепторы и липиды попадают в клетку, когда кавеола отпочковывается, образуя везикулу. Плазматическая мембрана также образует более крупные гетерогенные структуры, которые называются макропиносомы.
Обычно они образуются в ответ на действие факторов роста и представляют собой большие вакуоли, похожие по размеру на фагосомы. В них могут содержаться крупные капли внеклеточной жидкости. Материал, попавший в клетку с помощью кавеол и макропиносом, достигает тех же эндосом и лизосом, так же как и материал, поглощенный через окаймленные ямки. В некоторых случаях содержимое кавеол может храниться в специальной эндосоме, которая называется кавеосома. Наконец, некоторые метаболиты попадают в клетку вместе с мелкими пиноцитозными везикулами, которые образуются в отсутствие известных типов оболочек (окаймления).
Интересно, что некоторые вирусы животных используют кислые значения pH, характерные для эндоцитоза, для проникновения в цитоплазму клетки, где они проходят цикл репликации. Так, вирусы везикулярного стоматита и леса Семлики проникают в клетку через кислое окружение люмена эндосом; при этом активируются гликопротеины «шипов» на поверхности вирусной частицы и запускается процесс слияния мембран вируса и эндосомы. При этом происходит попадание в цитоплазму клетки вирусного генома и начинается распространение инфекции.
В клетках почкующихся дрожжей S. cerevisiae происходит пиноцитоз, но не фагоцитоз. Это не вызывает удивления, поскольку дрожжевая клетка обладает толстой клеточной стенкой. У этих клеток плохо различимы органеллы, принимающие участие в эндоцитозе, поскольку их очень мало. Однако вакуоли, которые представляют собой аналоги лизосом, хорошо видны в электронном микроскопе. До недавних пор генетические исследования эндоцитоза на дрожжах отставали от исследований экзоцитоза, и лишь в последнее время они стали особенно важны для понимания роли убиквитинирования белков в процессе их деградации.
В клетках иммунной системы специализированные лизосомы разрушают захваченные белковые антигены,
образуя пептиды, которые связываются с молекулами МНС класса II.
Комплексы пептид-МНС класса II транспортируются в плазматическую мембрану для представления антигена эффекторным клеткам. В поляризованной клетке процесс трансцитоза протекает таким образом,
что материал, транспортируемый по механизму эндоцитоза из одного мембранного домена,
проходит через клетку и путем экзоцитоза выходит через другой мембранный домен.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Фагоцитоз. Механизмы и значение фагоцитоза
Наиболее важной функцией нейтрофилов и макрофагов является фагоцитоз — поглощение клеткой вредоносного агента. Фагоциты избирательны в отношении материала, который они фагоцитируют; иначе они могли бы фагоцитировать нормальные клетки и структуры организма. Осуществление фагоцитоза зависит главным образом от трех специфических условий.
Во-первых, большинство естественных структур имеют гладкую поверхность, которая препятствует фагоцитозу. Но если поверхность неровная, возможность фагоцитирования возрастает.
Во-вторых, большинство естественных поверхностей имеют защитные белковые оболочки, отталкивающие фагоциты. С другой стороны, большинство погибших тканей и инородных частиц лишены защитных оболочек, что делает их объектом фагоцитоза.
В-третьих, иммунная система организма образует антитела против инфекционных агентов, например бактерий. Антитела прикрепляются к мембранам бактерий, и бактерии становятся особенно чувствительными к фагоцитозу. Для осуществления этой функции молекула антитела также соединяется с продуктом С3 каскада комплемента — дополнительной частью иммунной системы, обсуждаемой в отдельной статье на сайте (просим вас пользоваться формой поиска выше). Молекулы С3, в свою очередь, прикрепляются к рецепторам на мембране фагоцитов, инициируя фагоцитоз. Этот процесс выбора и фагоцитоза называют опсонизацией.
Переработка содержимого пиноцитозных и фагоцитарных вакуолей с помощью лизосомальных ферментов. Стадии фагоцитоза
а) Фагоцитоз, осуществляемый нейтрофилами. Нейтрофилы, входящие в ткани, являются уже зрелыми клетками, способными к немедленному фагоцитозу. При встрече с частицей, которая должна быть фагоцитирована, нейтрофил сначала прикрепляется к ней, а затем выпускает псевдоподии во всех направлениях вокруг частицы. На противоположной стороне частицы псевдоподии встречаются и сливаются друг с другом. При этом образуется замкнутая камера, содержащая фагоцитируемую частицу. Затем камера погружается в цитоплазматическую полость и отрывается от наружной стороны клеточной мембраны, формируя свободно плавающий фагоцитарный пузырек (также называемый фагосомои) внутри цитоплазмы. Один нейтрофил обычно может фагоцитировать от 3 до 20 бактерий, прежде чем он сам инактивируется или погибает.
б) Фагоцитоз, осуществляемый макрофагами. Макрофаги представляют собой конечную стадию развития моноцитов, входящих в ткани из крови. При активации иммунной системой они становятся гораздо более мощными фагоцитами, чем нейтрофилы, и часто могут фагоцитировать до 100 бактерий. Макрофаги также способны поглощать гораздо более крупные частицы, даже целые эритроциты и иногда малярийных паразитов, тогда как нейтрофилы не могут фагоцитировать частички, размер которых значительно превышает размер бактерии. Кроме того, макрофаги могут выталкивать конечные продукты и часто живут и функционируют в течение многих месяцев.
в) Сразу после фагоцитирования большинство частиц перевариваются внутриклеточными ферментами. После фагоцитирования инородной частицы лизосомы и другие цитоплазматические гранулы нейтрофила или макрофага немедленно вступают в контакт с фагоцитарным пузырьком, их мембраны сливаются, в результате в пузырек вбрасываются многие переваривающие ферменты и бактерицидные вещества. Таким образом, фагоцитарный пузырек теперь становится переваривающим пузырьком, и сразу начинается расщепление фагоцитированной частицы.
И нейтрофилы, и макрофаги содержат громадное количество лизосом, наполненных протеолитическими ферментами, особенно приспособленными для переваривания бактерий и других чужеродных белковых веществ. Лизосомы макрофагов (но не нейтрофилов) содержат также большое количество липаз, которые разрушают толстые липидные мембраны, покрывающие некоторые бактерии, например туберкулезную палочку.
г) И нейтрофилы, и макрофаги могут уничтожать бактерии. Кроме переваривания поглощенных бактерий в фагосомах нейтрофилы и макрофаги содержат бактерицидные агенты, уничтожающие большинство бактерий, даже если лизосомальные ферменты не могут их переварить. Это особенно важно, поскольку некоторые бактерии имеют защитные оболочки или другие факторы, предупреждающие их разрушение пищеварительными ферментами. Основная часть «убивающего» эффекта связана с действием некоторых мощных окислителей, образуемых в больших количествах ферментами мембраны фагосомы, или специфической органеллой, называемой пероксисомой. К этим окислителям относятся супероксид (О2 - ), пероксид водорода (Н2О2) и гидроксилъные ионы (-ОН), каждый из них даже в небольших количествах смертелен для большинства бактерий. Кроме того, один из лизосомальных ферментов — миелопероксидаза — катализирует реакцию между Н2О2 и ионами Cl с образованием гипохлорита — мощного бактерицидного агента.
Однако некоторые бактерии, особенно туберкулезная палочка, имеют оболочки, устойчивые к лизосомальному перевариванию, и к тому же секретируют вещества, отчасти препятствующие «убивающим» эффектам нейтрофилов и макрофагов. Такие бактерии ответственны за многие хронические болезни, например туберкулез.
Выводы
Сейчас микроглия активно изучается, и, хотя нам известно о ней далеко не все, обретенные нами знания уже дают новые шансы в лечении самых распространенных нейродегенеративных заболеваний. Поэтому дальнейшее изучение данной области может стать большим шагом для современной нейробиологии и медицины.
Опухоль и иммунитет — драматический диалог в трех частях с прологом
Долгое время считалось, что причина низкой эффективности иммунного ответа при раке — то, что опухолевые клетки слишком похожи на нормальные, здоровые, чтобы иммунная система, настроенная на поиск «чужаков», могла их как следует распознавать. Этим как раз и объясняется тот факт, что иммунная система успешнее всего противостоит опухолям вирусной природы (их частота резко возрастает у людей, страдающих иммунодефицитом). Однако позже стало ясно, что это не единственная причина.
Если в этой статье речь идет про иммунные аспекты рака, то в работе «Страшней клешней на свете нет. » [1] можно прочесть про особенности ракового метаболизма. — Ред.
Оказалось, что взаимодействие раковых клеток с иммунной системой носит гораздо более разносторонний характер. Опухоль не просто «прячется» от атак, она умеет активно подавлять местный иммунный ответ и перепрограммировать иммунные клетки, заставляя их обслуживать собственные злокачественные нужды.
«Диалог» между переродившейся, вышедшей из-под контроля клеткой с ее потомством (то есть будущей опухолью) и организмом развивается в несколько стадий, и если вначале инициатива почти всецело находится на стороне защитных сил организма, то в конце (в случае развития болезни) — переходит на сторону опухоли. Несколько лет назад учеными-онкоиммунологами была сформулирована концепция «иммуноредактирования» (immunoediting), описывающая основные этапы этого процесса (рис. 1) [2].

Рисунок 1. Иммуноредактирование (immunoediting) в процессе развития злокачественной опухоли.
Первая стадия иммуноредактирования — процесс устранения (elimination). Под действием внешних канцерогенных факторов или в результате мутаций нормальная клетка «трансформируется» — приобретает способность неограниченно делиться и не отвечать на регуляторные сигналы организма. Но при этом она, как правило, начинает синтезировать на своей поверхности особые «опухолевые антигены» и «сигналы опасности». Эти сигналы привлекают клетки иммунной системы, прежде всего макрофаги, натуральные киллеры и Т-клетки. В большинстве случаев они успешно уничтожают «испортившиеся» клетки, прерывая развитие опухоли. Однако иногда среди таких «предраковых» клеток оказывается несколько таких, у которых иммунореактивность — способность вызывать иммунный ответ — по каким-то причинам оказывается ослабленной, они синтезируют меньше опухолевых антигенов, хуже распознаются иммунной системой и, пережив первую волну иммунного ответа, продолжают делиться.
В этом случае взаимодействие опухоли с организмом выходит на вторую стадию, стадию равновесия (equilibrium). Здесь иммунная система уже не может полностью уничтожить опухоль, но еще в состоянии эффективно ограничивать ее рост. В таком «равновесном» (и не обнаруживаемом обычными методами диагностики) состоянии микроопухоли могут существовать в организме годами. Однако такие затаившиеся опухоли не статичны — свойства составляющих их клеток постепенно меняются под действием мутаций и последующего отбора: преимущество среди делящихся опухолевых клеток получают такие, которые способны лучше противостоять иммунной системе, и в конце концов в опухоли появляются клетки-иммуносупрессоры. Они в состоянии не только пассивно избегать уничтожения, но и активно подавлять иммунный ответ. По сути, это эволюционный процесс, в котором организм невольно «выводит» именно тот вид рака, который его убьет.
Этот драматический момент знаменует собой переход опухоли к третьей стадии развития — избегания (escape), — на которой опухоль уже малочувствительна к активности клеток иммунной системы, более того — обращает их активность себе на пользу. Она принимается расти и метастазировать. Именно такая опухоль обычно диагностируется медиками и изучается учеными — две предыдущие стадии протекают скрыто, и наши представления о них основаны главным образом на интерпретации целого ряда косвенных данных.
Читайте также:


