Скорость коррозии железа будет наибольшей при его контакте с алюминием хромом кобальтом медью
Обращаем Ваше внимание, что в соответствии с Федеральным законом N 273-ФЗ «Об образовании в Российской Федерации» в организациях, осуществляющих образовательную деятельность, организовывается обучение и воспитание обучающихся с ОВЗ как совместно с другими обучающимися, так и в отдельных классах или группах.
Рабочие листы и материалы для учителей и воспитателей
Более 2 500 дидактических материалов для школьного и домашнего обучения
- Онлайн
формат - Диплом
гособразца - Помощь в трудоустройстве
311 лекций для учителей,
воспитателей и психологов
Получите свидетельство
о просмотре прямо сейчас!
Урок по теме “Коррозия металлов. Способы защиты от коррозии”.
Место урока в теме «Металлы»: третий урок в теме
Оборудование: образцы изделий, подверженных коррозии, 5 стаканов с железным гвоздём, 1стакан - водопроводная вода, 2 стакан - вода с поваренной солью, 3 стакан - вода с поваренной солью и медная проволока, 4 стакан - вода с поваренной солью, алюминиевая проволока, 5 стакан - вода с поваренной солью, гидроксид натрия, оцинкованная пластинка, красная кровяная соль, жесть, кусочек консервной банки, таблицы “Виды коррозии”, “Методы защиты от коррозии”
Обучающая цель урока:
Организовать деятельность учащихся способствующую формированию представлений о сущности процесса коррозии металлов и способов их защиты от коррозии, классификации коррозионных процессов, методов защиты металлов от коррозии.
Личностно-развивающие задачи урока:
Способствовать развитию умений наблюдать, сравнивать, обобщать, делать самостоятельные выводы, работать в группах, развитию познавательного интереса к предмету;
обозначить экологические проблемы, связанные с коррозией металлов, рассмотреть влияние коррозии на здоровье человека. Объяснять происходящие явления, используя полученные знания.
Содействовать развитию коммуникативных умений, необходимых при работе в паре, в группе.
1.Организационный этап:
Приветствие. Учитель проверяет готовность учащихся к уроку.
Разбивает класс на группы(5 групп).
Метод четыре угла:
Распределение обязанностей: автоответчик, секретарь, хранитель времени, сомневающийся.
2. Ориентировачно- мотивационный этап:
Сегодня нам предстоит провести необычный урок-исследование. Классная доска на время станет исследовательским дневником, на ней мы будем записывать всё самое важное и нужное, что удаётся выяснить за время работы. А ваши тетради станут личными дневниками, не забывайте вести записи. Что же является объектом нашего исследования. Это коварный и давний, опасный враг большинства применяемых в технике и быту металлов. Днём и ночью он ведёт наступление на позиции своих недругов. Коварство этого извечного врага в том, что он невидимый, всегда остаётся целым и невредимым. А металлы и сплавы несут огромные потери.
Как вы уже догадались
Тема урока « Коррозия металлов ».
- что такое коррозия металлов?
- Какие виды коррозии бывают?
- Как протекает этот процесс?
-Какова роль коррозии в жизни человеческого общества и зачем ее изучать?
- Какие способы защиты от нее существуют?
Вот вопросы, на которые мы должны дать ответ к концу урока
Почему консервная банка
3.Операционно-познавательный этап
3.1.Работа в группах:
Каждая из групп получает задание и составляет опорную схему по своему блоку информации. (Приложение 2)
Задания групп:
1.Изучить материал учебника с.250 «Коррозия железа»
2.Ответить на вопросы:
-Что такое коррозия?
-Какие виды коррозии бывают?
1.Изучить материал учебника с.250-251 «Коррозия железа»
Факторы, влияющие на коррозию:
1.Изучить материал учебника с.251 «коррозия железа»
2.Ответить на вопрос:
-Как влияет контакт железа с другими металлами на его коррозию?
Влияние на коррозию контакта с другими металлами:
Fe /более активный металл ?
Fe /менее активный металл ?
1.Изучить материал учебника с.251-252 «коррозия других металлов»
2.Ответить на вопросы:
-Подвергаются ли другие металлы коррозии?
- Какие металлы имеют высокую коррозионную стойкость?
В-ва вызывающие коррозию
1.Изучить материал учебника с.252 «защита от коррозии»
2.Ответить на вопрос:
-Как защитить металл от коррозии?
Пассивные методы: Активные методы:
3.2. Выступление групп
3.2.1Выступление групп и представление своих продуктов (схем)
3.2.1Выступление участников школьного научного общества и представление своих результатов:
Группа учащихся вашего класса, готовясь к школьной научно-практической конференции, работала над темой «Исследование влияния сред, контактов металлов на скорость коррозии ». Я попрошу их поделится своими результатами .
Практическая часть.(выступление учащихся)
При использовании металлических материалов очень важен вопрос о скорости их коррозии. Для того, что бы убедиться, мы решили провести опыт в различных средах и с различными металлами. Для проведения опыта мы приготовили 5 стаканов и 5 железных гвоздей.
1-й стакан – заполнили обыкновенной водопроводной водой и опустили в него гвоздь.
2-й стакан – заполнили водопроводной водой, добавили поваренной соли и опустили в него гвоздь.
3-й стакан – заполнили водопроводной водой с поваренной солью, к гвоздю прикрепили медную проволоку и опустили в стакан.
4-й стакан - заполнили водопроводной водой с поваренной солью, к гвоздю прикрепили предварительно зачищенную наждачной бумагой алюминиевую проволоку и опустили в стакан.
5й стакан - заполнили водопроводной водой с поваренной солью, добавили в раствор гидроксид натрия и опустили в него железный гвоздь.
1-й стакан – железо слабо коррозировало, в чистой воде коррозия идет медленнее, так как вода слабый электролит. В данном случае мы наблюдаем химическую коррозию.
2-й стакан – химическая коррозия. Но здесь скорость коррозии гораздо выше, чем в первом случае, следовательно, хлорид натрия увеличивает скорость коррозии.
3-й стакан – железный гвоздь в контакте с медной проволокой опущен в раствор хлорида натрия. Скорость коррозии очень велика, образовалось много ржавчины. Следовательно, хлорид натрия – это сильно коррозионная среда для железа, особенно в случае контакта с менее активным металлом – медью.
А (+) на железе на меди К (-)
4-й стакан – так же наблюдается коррозия железного гвоздя, алюминиевая проволока остается без изменений, хотя её перед началом опыта была очищена от оксидной пленки наждачной бумагой, вероятно, оксидная пленка образовалась снова.
5-й стакан – железный гвоздь опущен в раствор хлорида натрия, к которому добавили гидроксид натрия. Коррозия железа в данном случае отсутствует.
Выводы: Мы убедились на опыте, что коррозию железа можно уменьшить с помощью гидроксида натрия. Он замедляет процесс коррозии, а гидроксид анионы являются ингибиторами, то есть замедлителями коррозии. Из наших наблюдений можно сделать вывод, что алюминий для протекторной защиты использовать нельзя, так как железо все равно разрушается.
3.3Демонстрационный эксперимент учителя.
Используя ПСХЭ, сравните коррозионные свойства металлов?
Какова эффективность защиты от коррозии некоторых металлических покрытий?
В два стакана с раствором соляной или серной кислот и красной кровяной соли кладутся пластинки.
В первый стакан белая жесть (луженое железо), во второй стакан оцинкованная жесть.
В первом стакане изменился цвет, т.е. железо разрушается. Вот почему луженый бак в местах повреждения быстро ржавеет, а оцинкованный при этих же условиях не разрушается.
Проблема коррозии появилась, как только появился первый металл. Очевидно, её никогда не удастся разрешить полностью, и самое большое, на что можно рассчитывать в настоящее время – это замедлить “Возвращение металлов к природе”.
Великий Гёте сказал: “Просто знать ещё не всё, знания нужно уметь использовать”.
3.4. Решение проблемных ситуаций в группах:
«Проблемные ситуации – причины и последствия коррозии»
Колосс Родосский
В III до нашей эры на острове Родос был построен маяк в виде огромной статуи Гелиоса. У Колосса Родосского бронзовая оболочка была смонтирована на железном каркасе. Колосс Родосский считался одним из семи чудес света, однако просуществовал всего 66 лет и рухнул во время землетрясения. Ученые считают, что причиной произошедших событий были окислительно-восстановительные процессы. Какие именно?
Яхта миллионера.
В 20-е годы ХХ в. с одним американским миллионером произошла неприятная история. По его заказу была построена роскошная яхта “Зов моря”. Для обшивки корпуса яхты использовался сплав никеля с медью, известный под названием монель-металл. Этот сплав отличался чрезвычайно высокой стойкостью во многих агрессивных средах, в том числе и в морской воде. Другие детали корпуса судна были изготовлены из специальных нержавеющих сталей, т.е. материалов, содержащих железо. Когда яхта была спущена на воду, судно затонуло, ни сделав, ни одного рейса. Поясните почему.
Проблемы стоматологии
Иногда зубные коронки, изготовленные из различных металлов (золота и стали) и близко расположенные друг к другу, доставляют их носителям неприятнейшие болевые ощущения. Пациенты часто жалуются на резкую зубную боль. С чем это связано?
Символ Парижа.
Символом Парижа – Эйфелева башня. Стальной каркас 300 метровой конструкции выполнен из сталей с различными добавками. Она неизлечимо больна, ржавеет и разрушается, и только постоянная химиотерапия помогает бороться с этим смертельным недугом: Её красили 18 раз, отчего её масса 9000 т каждый раз увеличивается на 70 т. Ученые считают, что причиной разрушений являются окислительно-восстановительные процессы. Какие именно?
4.Контрольно-коррекционный этап:
Выполнение теста . (Приложение 1)
Ответы к тесту: 1б 2б,г 3б 4а 5в,г 6в 7а,б,д 8в 9в 10 б,г,д
5. Рефлексия:
Возвратимся к поставленным вопросам в начале урока, на все ли вопросы вы можете ответить?
- Что такое коррозия металлов?
- Какие виды коррозии бывают?
- Как протекает этот процесс?
-Какова роль коррозии в жизни человеческого общества и зачем ее изучать?
- Какие способы защиты от коррозии существуют?
И так мы закончили наше исследование, надеюсь, оно вам принесло много интересного и познавательного.
6. Домашнее задание
Для любознательных подготовить презентацию на тему “Коррозия - друг и враг”.
Рассмотрим коррозию железа, находящегося в контакте с медью в кислой среде, например водном растворе НС1(рис.11). В образующемся гальваническом элементе анодом является железо (Е° Fe/Fe2+ = -0,44 В), а като-
Рисунок 11- Коррозии железа при контакте с медью в кислой среде (рН <7)
Следовательно, железо на поверхности окисляется, образующиеся при этом свободные электроны перемещаются от железа к меди (на катод), где участвуют в процессе восстановления ионов водорода (Н + ), находящихся в электролите (рН < 7):
Анод: Fe│ Fe° - 2 е → Fe 2+
Катод: Сu | 2Н + +2 ё → Н2
Если в электролите не содержится кислоты (рН > 7), то анодный процесс не изменится, но на катоде будет восстанавливаться растворённый в воде кислород:
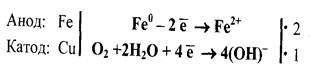
При контакте железа с металлом, имеющим меньший потенциал, например с цинком (E°Zn/Zn2+ = - 0,76 В), в возникающем гальваническомэлементе анодом будет являться цинк, а катодом - железо. Коррозии в данном случае будет подвергаться цинк, а железо разрушаться не будет, так как катодные реакции не затрагивают металл катода:
Анод: Zn│Zn° - 2 ё → Zn 2+
Катод: Fe │2Н + + 2 ё → Н2 (в кислой среде),
Анод:Zn│Zn° - 2 ё → Zn│2
Катод: Fe │О2+2Н2О + 4ё →4(ОН) - │1(в отсутствие кислоты)
Таким образом, контакт с цинком предотвращает коррозию железа, что часто используется для защиты стальных изделий от коррозии. Соединения металлов в сплавах также обладают электропроводностью, а следовательно, могут участвовать в работе гальванических элементов.
Рассмотрим атмосферную коррозию стали (рис. 12).
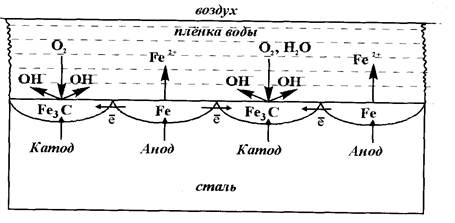
Рисунок 12 - Атмосферная коррозия стали
В составе стали всегда имеются кристаллиты феррита (железо) и цементита (карбид железа - Fe3C). Так как Е°Fе< Е°Fе3С , то при наличии влаги (электролита) на поверхности стали между кристаллами Fe и Fe3C возникает множество микрогальванических элементов, в которых анодом будут частицы железа (феррита), а катодом - кристаллиты цементита:
Анод:Fe │Fe° - 2 ё → Fe 2+ │2
Образующиеся на аноде и катоде ионы соединяются в нерастворимый гидроксид:
который быстро окисляется кислородом воздуха:
Получающийся таким образом Fe(OH)3 составляет основу ржавчины.При высыхании он может частично или полностью терять воду, превращаясь в метагидроксид FeO(OH), или Fe2О3. Ржавчина представляет собой бурый, рыхлый налет, не защищающий металл от дальнейшего разрушения.
2) Коррозия при неравномерной аэрации разных участков поверхности одного металла
Неравномерная аэрация означает неодинаковое содержание кислорода воздуха в электролите (воде) у разных участков поверхности металла. Известно, что с ростом концентрации растворённого в электролите (воде) кислорода, возрастает и значение электродного потенциала металла.
Если на гладкую железную пластинку нанести каплю водного раствора соли (например, NaCl), то по краям капли (там, где кислорода больше) образуются катодные участки, а анод будет находиться там, где содержание кислорода меньше всего - в центре капли. Там же (на аноде) будет происходить окисление, то есть коррозия железа. По краям капли на поверхности железной пластинки происходит восстановление кислорода с образованием ионов ОН - . Эти ионы образуют с ионами железа нерастворимые гидроксиды (ржавчина) в виде колец между центром и краями капли, как показано на рис.13.
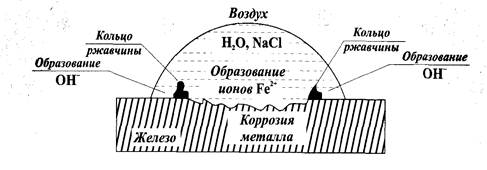
Рисунок 13 - Коррозия железа в условиях неравномерной аэрации
Запишем анодный и катодный процессы:
Анод: Fe - центр капли│Fe° - 2 ё → Fe 2+ │2
Катод: Fe - край капли│О2+2Н2О + 4ё →4(ОН) - │1
Аналогичные процессы будут происходить и в других случаях неравномерной аэрации: коррозии в первую очередь подвергается тот участок поверхности металла, доступ кислорода воздуха к которому затруднён.
3) Коррозия под действием блуждающих токов
Источником подземных блуждающих токов могут быть различные устройства, работающие на постоянном токе. Это электропоезда, метро, трамваи, троллейбусы, установки для электросварки, электролизёры и т.д. Коррозию под действием внешнего источника электрического тока называют электрокоррозией.

Рассмотрим коррозию подземного стального трубопровода во влажной почве под действием блуждающих токов (рис.14).
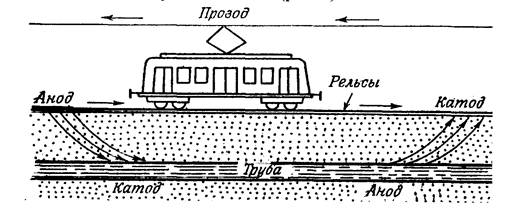
Рисунок 14 - Коррозия подземных коммуникаций под действием блуждающих токов
В месте входа тока в трубопровод возникает катодный участок, и на этом участке будет протекать реакция восстановления молекулярного кислорода, находящегося во влажной почве. Участок металла трубопровода, где происходит выход тока, становится анодом и разрушается.
Запишем анодный и катодный процессы:
Анод: Fe│Fe° - 2 ё → Fe 2+ │2
Коррозия под действием блуждающих токов обычно приводит к быстрому разрушению подземных металлических конструкций.
6. Как ведет себя алюминий в высококонцентрированной азотной кислоте?
7. Как изменится скорость коррозии при загрязнение поверхности алюминия благородными металлами?
8. Чем объясняется неустойчивость меди и медных сплавов в аммиачных растворах?
9. Скорость коррозии цинка выше: во влажном воздухе; в воде, содержащей углекислый газ; сухой атмосфере; воде, содержащей кислород
10. Более устойчив к коррозии алюминий, содержащий примесь: магния, никеля, серебра, кобальта
11. Для предотвращения коррозии сталей и сплавов при высоких температурах применяют: (тип защиты)
12. Под действием электрического тока коррозионный процесс происходит: (на катоде или на аноде)
13. Быстрее всего стальные конструкции корродируют в среде: (рН среды)
14. Электрокоррозией называют коррозию под действием:
15. При избирательной коррозии в окисленное состояние переходит ----- металл: (более или менее активный)
16. Коррозия стали в почве является: (тип коррозии)
17. Наиболее коррозионноопасной для стальной конструкции является вода, содержащая растворенный: хлорид натрия, бром, сульфид натрия, раствор аммиака
18. Электрохимическая коррозия протекает в: нефти, кислоте, этаноле
19. Химическая коррозия протекает в растворе: соляной кислоты, брома в эфире, СО2 в воде
20. Что такое оксидирование?
21. Химическая коррозия протекает в среде: хлороводород (газ), хлороводород (раствор в воде), бром (раствор в воде)
22. Сплав меди с цинком называется латунью. Что происходит при коррозии латуни?
23. Менее опасным с точки зрения коррозии железа является раствор, рН которого: 2, 4, 7, 10
24. Наиболее интенсивно коррозия железа протекает в растворе, содержащем: хлорид натрия, фосфат калия, хлорид цинка
25. Чем объясняется значительная стойкость алюминия к коррозии?
26. Для защиты стальной конструкции от коррозии на ее поверхности следует закрепить пластину: магниевую, кобальтовую, из висмута
27. Для защиты металлов от коррозии наносят металлические покрытия. В случае
нарушения целостности покрытия оловянного стального изделия происходит:
28. На поверхности закисленной почвы садового участка находятся железные трубы с никелевыми кранами. Коррозии будет подвергаться:
29. Катодно хром поляризуется в контакте с: цинком, серебром, алюминием
30. Медь поляризуется анодно в контакте с: цинком, железом, золотом
31. Коррозия олова с водородной деполяризацией возможна в растворе с рН: 3, 7 ,12
32. Коррозия железа с водородной деполяризацией возможна в растворе с рН: 5, 7, 11
33. Быстрее всего железо будет корродировать в контакте с: алюминием, серебром, медью
34. Что такое легирование? Каково его назначение?
35. В качестве протектора для защиты медной конструкции от коррозии можно использовать: серебро, никель, смолу
36. С какой целью используют ингибиторы?
37. Какие покрытия называют катодными?
38. Какие покрытия называют анодными?
39. Протектором для защиты стальной конструкции от коррозии может быть: платина, хром, никель
40. Коррозионноопасными называют покрытия металлами, потенциал которых (больше, меньше, равны) потенциала основного металла
41. Покрытие железа кобальтом является коррозионноопасным, так как: это покрытие анодное, кобальт вообще не защищает от коррозии, это покрытие катодное, никель быстро окисляется
42. Для защиты стальной конструкции от коррозии в качестве протектора использовали магний. Анодный процесс при коррозии такой системы в кислой среде представляет собой: Fe - 2ē → Fe 2+ , Н2О - 2ē → ½ О2 + 2 Н + , 2Н + + 2ē → Н2,Mg - 2ē → Mg 2+
43 Как достигается катодная защита металлов от коррозии?
44. Электрохимическая коррозия металла возможна при условии, что потенциалокислителя (больше, меньше, равен) потенциала металла:
45. Как изменяется скорость катодного процесса при коррозии с водородной деполяризацией с уменьшением величины рН?

46. Как изменяется скорость катодного процесса при коррозии металлов в кислой среде с увеличением водородного перенапряжения?
47. Как изменяется скорость коррозионного процесса в нейтральной среде с кислородной деполяризацией при повышении температуры выше 80 °С?
49. Катодный процесс с кислородной деполяризацией при коррозии в нейтральной среде представляет собой: 2Н2О + 2ē → Н2 + 2ОН - , 2Н2О - 4ē → О2 + 4Н + , О2 + 4Н + + 4ē → 2Н2О, О2 + 2Н2О + 4ē → 4ОН -
50. Присутствие ионов хлора в коррозионной среде ускоряет коррозию, так как: затрудняется переход ионов металла в раствор, ионы хлора активируют пассиваторы, ионы хлора активируют ингибиторы, хлориды металлов легко растворяются.
51. Что является лимитирующей стадией коррозионного процесса, идущего с кислородной деполяризацией?
52. Что представляет собой анодный процесс коррозии контакта Sn / Ag, протекающей с водородной деполяризацией?
53. Стальная деталь покрыта оловом. Что представляет собой анодный процесс коррозии в кислой среде при нарушении целостности покрытия?
54. В щелочной среде в присутствии кислорода возможна коррозия: серебра, меди, ртути, платины
55. В нейтральной среде в отсутствии кислорода термодинамически устойчив: магний, алюминий, олово, цинк
56. В нейтральной среде в отсутствии кислорода термодинамически неустойчив: медь, хром, никель, серебро
Обращаем Ваше внимание, что в соответствии с Федеральным законом N 273-ФЗ «Об образовании в Российской Федерации» в организациях, осуществляющих образовательную деятельность, организовывается обучение и воспитание обучающихся с ОВЗ как совместно с другими обучающимися, так и в отдельных классах или группах.
Рабочие листы и материалы для учителей и воспитателей
Более 2 500 дидактических материалов для школьного и домашнего обучения
- Онлайн
формат - Диплом
гособразца - Помощь в трудоустройстве
311 лекций для учителей,
воспитателей и психологов
Получите свидетельство
о просмотре прямо сейчас!

«Как закрыть гештальт: практики и упражнения»
Свидетельство и скидка на обучение каждому участнику
Описание презентации по отдельным слайдам:

Коррозия металлов «Коррозия – рыжая крыса, грызет металлический лом» В. Шефнер

У металлов есть враг, который приводит к огромным безвозвратным потерям металлов, ежегодно полностью разрушается около 10% производимого железа. По данным Института физической химии РАН, каждая шестая домна в России работает впустую – весь выплавляемый металл превращается в ржавчину. Этот враг - коррозия.

Проблема защиты металлов от коррозии возникла почти в самом начале их использования. Люди пытались защитить металлы от атмосферного воздействия с помощью жира, масел, а позднее и покрытием другими металлами и, прежде всего, легкоплавким оловом (лужением). В трудах древнегреческого историка Геродота (V в. до н.э.) уже имеется упоминание о применении олова для защиты железа от коррозии.

В III до нашей эры на острове Родос был построен маяк в виде огромной статуи Гелиоса. Колосс Родосский считался одним из семи чудес света, однако просуществовал всего 66 лет и рухнул во время землетрясения. У Колосса Родосского бронзовая оболочка была смонтирована на железном каркасе. Под действием влажного, насыщенного солями средиземноморского воздуха железный каркас разрушился.

В 20 годы ХХ в. по заказу одного миллионера была построена роскошная яхта “Зов моря”. Еще до выхода в открытое море яхта полностью вышла из строя. Причиной была контактная коррозия. Днище яхты было обшито медно-никелевым сплавом, а рама руля, киль и другие детали изготовлены из стали. Когда яхта была спущена на воду. Возник гигантский гальванический элемент, состоящий из катода- днища, стального анода и электролита – морской воды. В результате судно затонуло, ни сделав ни одного рейса.

Что является символом Парижа? –Эйфелева башня. Она неизлечима больна, ржавеет и разрушается, и только постоянная химиотерапия помогает бороться с этим смертельным недугом: её красили 18 раз, отчего её масса 9000 т каждыйраз увеличивается на 70 т.

Тема: «Коррозия металлов. Способы защиты от коррозии»

В результате изучения темы ,вы будете способны: 1.Рассмотреть понятие – коррозия 2. Ознакомиться с причинами возникновения коррозии, способы защиты от коррозии и последствия, вызываемые процессами коррозии.


Коррозия – разрушение металлов и сплавов под воздействием окружающей среды. Слово коррозия происходит от латинского corrodere, что означает разъедать.



Коррозия (от лат. Corrodere - разъедать) – самопроизвольное разрушение металлов и сплавов под влиянием окружающей среды «Ржа ест железо» - русская народная поговорка Ржавление – коррозия железа и его сплавов Ежегодно в мире разрушается около ¼ произведенного железа

Причины возникновения коррозии Химические и электрохимические процессы окисления, происходящие на поверхности металлических тел при их взаимодействии с внешней средой (неметаллами, водой, оксидами углерода и серы, растворами кислот и солей, органическими веществами )


Электрохимическая Коррозия Химическая

Химическая коррозия Разрушение металлов и сплавов в результате их химического взаимодействия с веществами окружающей среды (сухие газы, органические жидкости – нефтепродукты, спирты) Происходит окисление металла без возникновения в цепи электрического тока На поверхности металла образуется оксидная пленка Например: образование железной окалины при взаимодействии материалов на основе железа при высокой температуре с кислородом: 3Fe + 2O2 → Fe3O4

Электрохимическая коррозия Разрушение металлов в среде электролита с возникновением внутри системы электрического тока (при контакте двух металлов или на поверхности одного металла, имеющего неоднородную поверхность) Химические процессы: окисление коррозируемого металла, отдача электронов Электрические процессы: перенос электронов с одного участка к другому

Сущность коррозии. Коррозия состоит из двух процессов: химического – это отдача электронов и электрического – это перенос электронов.

Закономерности коррозии: 1. Если соединены два разных металла, то коррозии подвергается только более активный, и пока он полностью не разрушится, менее активный защищён.

Закономерности коррозии: 2. Скорость коррозии тем больше, чем дальше друг от друга в ряду напряжений расположены соединённые металлы.

Скорость коррозии больше, чем дальше друг от друга расположены металлы в электрохимическом ряду напряжений металлов: более активный металл разрушается, предохраняя менее активный от коррозии

По виду коррозионной среды

Газовая Атмосферная Жидкостная Почвенная Блуждающими токами

Ущерб, наносимый коррозией Мировая потеря 20 млн. тонн металла в год Еще более значимы косвенные потери


Способы защиты от коррозии

Одним из наиболее распространенных способов защиты металлов от коррозии является нанесение на их поверхность защитных пленок: лака, краски, эмали.

Широко распространенным способом защиты металлов от коррозии является покрытие их слоем других металлов. Покрывающие металлы сами корродируют с малой скоростью, так как покрываются плотной оксидной пленкой. Производят покрытие цинком, никелем, хромом и др.

В повседневной жизни человек чаще всего встречается с покрытиями железа цинком и оловом. Листовое железо, покрытое цинком, называют оцинкованным железом, а покрытое оловом – белой жестью. Первое в больших количествах идет на кровли домов, а из второго изготавливают консервные банки.

Эйфелева башня Каждые 7 лет Эйфелеву башню, в целях защиты от коррозии, требуется заново красить. На это уходит около 57 тонн краски

Создание сплавов с антикоррозионными свойствами. Для этого в основной металл добавляют до 12% хрома, никеля, кобальта или меди.

Памятник Ю. А. Гагарину Памятник Ю. А. Гагарину облицован пластинками из титанового сплава, не подвергающегося коррозии

Ингибиторы – вещества, замедляющие или предотвращающие коррозию. Ингибиторы коррозии вводят в замкнутые системы охлаждения, в нефтепродукты, впрыскивают в газопроводы для снижения коррозии труб изнутри. Например: для предотвращения коррозии железа в серной кислоте к ней добавляют в качестве ингибитора азотную кислоту. . Для замедления коррозии вводятся ингибиторы, то есть меняется состав среды

Соединение защищаемого металлического сооружения проводником с куском более активного металла (протектором)

Последствия коррозии 1. Материальные потери; 2. Уменьшение надежности работы оборудования; 3.Простой производства из-за замены вышедшего из строя оборудования; 4. Загрязнение и снижение качества продукции; 5. Потери сырья и продукции (утечка нефти, газа, воды); 6. Энергетические затраты

Тренировочный тест 1. Слово “коррозия” в переводе с латинского означает: а) разрушать; б) разъедать; в) ржаветь. 2. Требуется скрепить железные детали. Каким металлом целесообразно воспользоваться а) медью; б) цинком; в) свинцом. 3. Окисление металла в среде неэлектролита: а) электрохимическая коррозия; б) язвенная коррозия; в) химическая коррозия. б в б

4. Разрушение металла, находящегося в контакте с другим металлом в присутствии водного раствора электролита: а) газовая коррозия; б) электрохимическая коррозия; в) химическая коррозия. 5. Эмалирование это: а) защитное неметаллическое покрытие металла; б) электрохимический метод защиты металлов от коррозии; в) способ придания красоты металлическому изделию. 6. Легирование это: а) специальное введение в сплав элементов, замедляющих процесс коррозии; б) покрытие железного листа слоем олова; в) создание контакта с более активным металлом. б а а

7. Вещества, замедляющие процесс коррозии называются: а) протекторы; б) электроды; в) ингибиторы. 8. Присоединение к защищаемому металлу другого, более активного металла называется: а) металлопокрытие; б) контактная защита; в) протекторная защита. 9. Процесс ржавления металла можно наблюдать при коррозии: а) железа; б) алюминия; в) цинка. в в а

10. Некоторые металлы не подвергаются коррозии, т.к. они покрыты: а) защитным покрытием; б) водонепроницаемым покрытием; в) оксидной плёнкой. 11. Для протекания электрохимической коррозии необходимо наличие: а) воздуха; б) раствора электролита; в) органического растворителя. 12. Для протекания химической коррозии необходимо наличие: а) воздуха; б) раствора электролита; в) органического растворителя. а б а

Творческие задачи 1. Скульптуры из бронзы создавались еще в глубокой древности. В XIX веке для отливки статуй начали применять чугун (например, памятник князю Владимиру в Киеве). XX век вооружал скульпторов нержавеющей сталью и титаном (монумент покорителям космоса в Москве). Какой из перечисленных материалов в наибольшей степени подвержен коррозии, а какой – в наименьшей?

2. Почему поверхность статуи, отлитой из бронзы, содержащей даже незначительное количество цинка, со временем покрывается белыми точками? 3. Стоматологи не рекомендуют рядом со стальной коронкой (Fе) ставить золотую (Аu). Объясните их позицию с точки зрения протекающих процессов.

4. В III до нашей эры на острове Родос был построен маяк в виде огромной статуи Гелиоса. У Колосса Родосского бронзовая оболочка была смонтирована на железном каркасе. Колосс Родосский считался одним из семи чудес света, однако просуществовал всего 66 лет и рухнул во время землетрясения. С чем связана столь скоротечная жизнь этого чуда света?

Домашнее задание § … упр. № … Дополнительное задание № 1: Склёпаны 2 металла. Укажите, какой из металлов подвергается коррозии а) Mn – Al; б) Sn – Zn Дополнительное задание № 2: Образец латуни (медь + цинк) массой 200 грамм с массовой долей меди 60 % обработали избытком соляной кислоты. Определите объём газа, который выделится (н.у.)
Обращаем Ваше внимание, что в соответствии с Федеральным законом N 273-ФЗ «Об образовании в Российской Федерации» в организациях, осуществляющих образовательную деятельность, организовывается обучение и воспитание обучающихся с ОВЗ как совместно с другими обучающимися, так и в отдельных классах или группах.
Рабочие листы и материалы для учителей и воспитателей
Более 2 500 дидактических материалов для школьного и домашнего обучения
- Онлайн
формат - Диплом
гособразца - Помощь в трудоустройстве
311 лекций для учителей,
воспитателей и психологов
Получите свидетельство
о просмотре прямо сейчас!
муниципальное бюджетное общеобразовательное учреждение
средняя общеобразовательная школа № 58
Научно-практическая конференция учащихся
Опытно – экспериментальная работа на тему:
«Изучение влияния среды
на степень коррозии металлов»
ученик 9 «А» класса
Руководитель
МБОУ СОШ № 58 г. Пензы
Глава 1. История изучения коррозии металлов……………………………………5
1.1 Современное понятие о коррозии……………………………………………..6
Глава 2. Экспериментальные исследования…………………………………. 10
2.1 Изучение зависимости скорости коррозии
от присутствия кислорода ……………………………………………………..10
2.2 Изучение влияния электролитов на процесс коррозии……………………….11
2.3 Изучение влияния ингибиторов на процесс коррозии………………………..13
2.4 Экспериментальная часть по созданию «шиферного гвоздя»………………..14
Список использованной литературы……………………………………………….17
Жизнь человека без металлов невозможна. Лучше всего об этом написал Сычев А.П. и Фадеев Г.Н. в своей книге «Химия металлов»: [4]
Потери от коррозии колоссальны. Каждая шестая домна работает лишь для того, чтобы восполнить потери металлов, «съеденных» ржавчиной. Но вред, наносимый коррозией, не сводится только к потере металла вследствие его разрушения (прямые потери), больший вред наносят косвенные потери. Гибнет труд людей, затраченный на обработку металла и создание тех или иных машин и механизмов. Кроме того, немало труда приходится затратить, чтобы заменить «изъеденные» коррозией детали новыми. Например, для замены проржавевших под землей водопроводных труб приходится копать глубокие траншеи. В городе для этого надо сначала взломать асфальт, который лишь иногда лишь недавно был уложен. Чтобы сменить детали, например, химических или нефтехимических аппаратов, приходится останавливать производство, а вынужденная остановка даже на сутки обходится большими потерями готовой продукции. При коррозии загрязняется окружающая среда (например, за счет утечки газа, нефти), может произойти снижение качества или порча выпускаемой продукции и т.д. Таким образом, потери от коррозии в сотни раз превосходят стоимость металла. [1,3]
Актуальность: в промышленно развитых странах коррозия металлов наносит существенный ущерб экономике каждого государства, поэтому данные вопросы играют немаловажную роль как в быту, так и в масштабах целого государства. Проблема коррозии металла сопровождает человека с того самого момента, как человек научился изготавливать из металла предметы и орудия труда. Каждая шестая домна работает лишь для того, чтобы восполнить потери металлов, «съеденных» ржавчиной.
Гипотеза: при помещении железа в щелочную среду скорость коррозии уменьшится.
Новизна: в ходе проведения эксперимента выяснили, что железо в контакте с алюминием, как более активным металлом, коррозии практически не подвергается. Это позволило нам изготовить «шиферный гвоздь» гвоздь, более устойчивый к коррозии во внешней среде.
Объект исследования: железные гвозди
Предмет исследования: влияние условий на степень коррозии железа
Площадка проведения эксперимента: лаборатория МБОУ СОШ № 58 города Пензы.
Цель: исследовать действие факторов окружающей среды на степень коррозии железа.
Читайте также:


