Компьютерное моделирование работы органов что позволяет выявить
До настоящего времени основной сферой применения САПР являлись различные отрасли машиностроения, промышленные системы. Для решения медицинских и биологических задач САПР еще не применялись. Представляем вашему вниманию работу, выполненную сотрудниками Медицинской академии последипломного образования с помощью представительства фирмы Delcam plc (Великобритания) в Санкт-Петербурге.
Целью этой работы являлось создание трехмерной компьютерной модели органов шеи, груди и живота, которая позволила бы ответить на большинство вопросов, встающих перед хирургом при проведении операций на щитовидной железе, легких, печени, желудке и желчном пузыре. Для решения задач оперативной хирургии на базе системы DUCT фирмы Delcam plc был разработан объемный компьютерный атлас анатомии легких, верхнего этажа брюшной полости и органов шеи.
Строение внутренних органов и систем, а тем более целых анатомических областей, таких как шея, грудь и живот, является очень сложным. Выполнение любого хирургического вмешательства требует точного представления о деталях анатомических соотношений отдельных артерий, вен, нервов, желчных протоков, частей бронхиального дерева.
Любые операции на легких основаны на точном знании пространственных особенностей строения. В то же время строение легких в высшей степени вариабельно, а элементы строения — артерии и вены, которые приходится перевязывать или оставлять без пересечения, — расположены так близко друг к другу, что вероятность их неправильной идентификации очень велика. Выполнение сложных реконструктивных оперативных вмешательств на трахее и бронхах требует учета индивидуальных особенностей человека. Диагностические пункции опухолей легких через грудную стенку требуют аналитически точного описания строения и расчета с высокой степенью точности, чтобы не повредить при проколе легочные артерии и вены.
Специфика оперативных вмешательств на органах живота иная. Сосудов и анатомических вариантов здесь значительно меньше, чем в легких. Однако при выполнении операции лапароскопическим методом все манипуляции осуществляются в ограниченном поле зрения через полые трубки, без возможности определить анатомические элементы на ощупь. Кроме того, при лапароскопических операциях резко возрастает риск повреждения отдельных сосудов. Повреждение сосуда даже малого диаметра из-за трудноустранимого кровотечения требует прекращения эндовидеохирургической операции и перехода на выполнение ее открытым методом.
Область шеи характеризуется тем, что в ней располагаются жизненно важные органы и структуры: гортань, трахея, пищевод, сонные артерии и яремные вены, щитовидная железа, множество ветвей сосудов и нервов не только самой шеи, но и тех, которые распространяются на верхние конечности. Сложность операций на шее определяется не только непосредственной близостью органов и других анатомических структур друг к другу, но и особой подвижностью и смещаемостью этих структур, нарушающей привычные хирургу соотношения. Указанные особенности могут быть смоделированы на соответствующих компьютерных моделях и просмотрены как в процессе подготовки, так и непосредственно перед операцией.
В процессе подготовки к оперативному вмешательству хирург использует все доступные ему графические материалы, чаще всего содержащиеся в атласах и руководствах. Однако имеющиеся атласы из всех возможных вариантов строения содержат только часть наиболее типичных, к тому же представленных в двухмерном изображении.
В то же время современные способы диагностики с использованием ультразвука, компьютерной томографии, ядерного магнитного резонанса позволяют определить локализацию патологического очага с точностью до 1 мм. Чаще всего результатом исследований является срез по плоскости, проходящий через этот очаг и содержащий изображения артерий, вен, нервов и других элементов, лежащих в данном срезе. Однако опознать большинство из них не представляется возможным вследствие подобия форм и размеров. Получение трехмерных реконструкций при данных методах обследования возможно, но воспроизвести полученную трехмерную модель на персональном компьютере нельзя вследствие избыточного объема информации.
Для решения задач биологии и медицины разработано множество компьютерных пакетов, содержащих изображения внутренних органов, сосудов и нервов, других анатомических структур. Компьютерные модели, используемые в пакетах, как правило, двухмерные, но встречаются и трехмерные реконструкции. Последние содержат такие программы, как 3D-Body Adventure (США), Advantage Windows (США), ADAM (Великобритания), Corps Human (Франция). Наиболее известная программа Body Voyage (США), созданная в рамках исследования Visible Human Project (США), была построена по данным 1800 одномиллиметровых поперечных срезов человеческого тела. Точечная трехмерная модель тела человека потребовала 15 Гбайт компьютерной памяти. В основе большинства указанных программ лежит использование художественных графических пакетов с записью всех точек всех поверхностей в пространстве.
Основным требованием, которому должны отвечать компьютерные модели строения человека, является количество анатомических элементов, составляющих каждый внутренний орган. Необходимо наличие графических образов различных анатомических вариантов, так как типичные варианты специалистам хорошо известны. Если каждый анатомический элемент представлен в компьютерной модели в виде отдельного пространственного тела, возможно динамическое моделирование различных операций.
Известные пакеты отвечают этим требованиям в очень малой степени. Для них характерны ограниченные возможности построения виртуальных моделей, освоения хирургической техники, рассмотрения моделей на разных этапах операции. В то же время использование систем трехмерного поверхностного моделирования, применяемых в машиностроении (CAD/CAM-системы), позволяет реализовать эти требования.
Как во всех подобных исследованиях, конкретные данные были получены при изучении анатомических материалов. Все анатомические структуры легких (бронхи, артерии и вены легких) были представлены в аналитической форме, характеризующей их пространственное положение. Для создания компьютерной модели органов груди в аналитической форме было записано положение аорты, пищевода, трахеи, сердца и магистральных сосудов. Полученные показатели характеризовали не только типовое строение легких, но и множество анатомических вариантов, то есть то, что наиболее важно для хирурга. Аналитическое описание анатомии легких послужило основой построения их трехмерной компьютерной модели.
Трехмерная графическая компьютерная модель, содержащая несколько десятков вариантов строения правого и левого легкого, была выполнена с помощью пакета DUCT. Вследствие сложной пространственной локализации сосудов легких с большим количеством изгибов модель каждой артерии или вены содержала не менее пяти промежуточных сечений. Бронхи не имеют изгибов, поэтому для каждого бронха потребовалось записать только два сечения. Разветвления бронхов моделировались с помощью стандартной процедуры, имеющейся в исходном пакете. Разработанная модель позволила последовательно воспроизвести отдельные бронхи, бронхиальное дерево целиком, а затем в уже готовое изображение встроить ветви легочных артерий и вен с учетом реальной трехмерной структуры легких. Такая модель позволяет при подготовке легко запомнить, а в ходе операции опознать все анатомические элементы сложной структуры.
Компьютерное моделирование органов брюшной полости, особенно верхнего этажа брюшной полости, было направлено на решение задач, выдвигаемых при выполнении различных операций на желчном пузыре, печени и желудке. Так же как и в случае легких, моделирование основывалось на морфометрии анатомических материалов. Компьютерная модель печени воспроизвела очень сложный рельеф поверхности органа. В системе DUCT5 были смоделированы все известные варианты строения сосудов и желчных протоков, на которых осуществляется операция удаления желчного пузыря и правильность определения которых обеспечивает успех или неудачу при выполнении операции. Основным направлением в данном случае является применение модели при планировании лапароскопических холецистэктомий, в определении точек введения инструментов, в воспроизведении хода этой операции, в компьютерном отображении индивидуального строения желчных протоков по данным холангиографии.
Виртуальная модель шеи была разработана для обучения прежде всего операциям на щитовидной железе. В этой модели отразились не только особенности топографии сосудов и нервов по отношению к железе, но и конфигурация железы, соответствующая определенной степени ее диффузного увеличения.
Вид изображения, максимально имитирующий естественный, был получен благодаря имеющимся в пакете DUCT5 средствам окрашивания (материал, цвет, количество и расположение источников света). Для окрашивания сосудов были подобраны характерные для оригинала оттенки красного цвета, коэффициенты отражения и полировки материала. Желчный пузырь и желчные протоки получили окраску зеленого цвета. Окрашивание бронхов выполнено в оттенках белого, серого и черного цветов чередованием горизонтальных полос. Все трехмерные компьютерные модели отобразили многослойную структуру органов, с учетом индивидуальных особенностей анатомического строения.
Разработанные в пакете DUCT5 трехмерные модели с помощью гибких средств редактирования и модификации поверхностей позволили имитировать произвольные пространственные трансформации, моделировать возможные смещения анатомических структур во время операций. Это существенно отличает полученные модели от графических мультимедийных приложений.
Компьютерная анатомия, отражающая трехмерное анатомическое строение, была использована для разработки системы виртуального моделирования операций с позиции анатомических и технических обоснований. Повороты графических моделей органов на произвольный угол вокруг выбранной оси, применение операций масштабирования обеспечили воспроизведение архитектоники сосудов, бронхов и желчных протоков из различных хирургических доступов или одновременно из нескольких. Многооконный режим работы пакета DUCT позволил сопоставлять в разных окнах дисплея ход операции при разных вариантах анатомического строения и разных способах ее выполнения.
В настоящей разработке была использована возможность пакета DUCT5 размещать различные фрагменты модели на разных слоях, а затем послойно визуализировать эту «многослойную» модель, в нашем случае состоящую из отдельных очень важных анатомических элементов. Встроенный командный язык позволил написать командные файлы для управления процессом визуализации. В результате на базе синтезированной трехмерной модели были получены программы моделирования этапов операций на легких, желчном пузыре, щитовидной железе с последовательным удалением и добавлением анатомических элементов. Моделирование хода операций в трехмерной среде DUCT позволяет заранее определить возможные опасности хирургического вмешательства при разных способах его выполнения и особых вариантах анатомического строения. Только использование трехмерной многослойной модели позволяет предвидеть хирургические опасности, связанные с повреждением артерии, вены, желчного протока, располагающихся в глубине тканей, что может привести к тяжелому кровотечению и в конечном счете к проведению операции значительно большего объема.
Применение трехмерного моделирования позволило проводить измерения длин, углов и диаметров всех анатомических элементов в исходном состоянии и при пространственных трансформациях, что имеет существенное значение в оценке выполнимости сложных реконструктивных вмешательств, в определении оптимального способа. Вследствие получения по данным инструментальных исследований длину проекции анатомического элемента на перпендикулярные плоскости, в трехмерной модели органа имеется возможность определить длину самого элемента. Для проведения биопсии органов с помощью компьютерной модели вычисляются необходимые расстояние и угол, определяются координаты для выполнения прецизионных пункций.
Разработанные трехмерные компьютерные модели позволили провести структурный графический анализ строения органов, определить закономерности формирования множества вариантов их строения. Выявление таких закономерностей строения позволяет определить оптимальную технику выполнения различных вмешательств, исходя из конкретной, а не усредненной пространственной конфигурации.
Разработанные трехмерные компьютерные модели, выполненные с применением системы DUCT5, были использованы в процессе последипломного обучения врачей. Тестирование врачей-хирургов показало, что эффективность использования компьютерной анатомии данного типа в обучении в 2,5 раза выше, чем традиционных средств.
Таким образом, виртуальная картина органов и областей тела человека, полученная с помощью системы трехмерного моделирования DUCT5, соответствует анатомическому строению. Синтезированные компьютерные модели служат основой для решения задач предоперационного планирования и моделирования хода будущей операции с учетом многих технических и анатомических особенностей. Разработанная система обладает информационными возможностями, которые можно использовать в учебном процессе по анатомии и оперативной хирургии любой области человеческого тела, для создания интерактивных компьютерных атласов и учебных курсов. Имеющаяся в пакете DUCT5 возможность записи моделей в формате VRML позволяет использовать ее в глобальной сети Internet, применяя, например, пакет Cosmo Player. Это позволяет широко использовать данные разработки как справочные пособия в хирургических отделениях и хирургических центрах.
С выходом новой версии системы трехмерного моделирования фирмы Delcam plc — PowerSHAPE — возможности использования описанных разработок в медицинских учреждениях значительно расширились: стандартный персональный компьютер с операционной системой Microsoft Windows NT в качестве рабочей станции; очень простой графический интерфейс пользователя, основанный на технологии интеллектуального курсора; возможность обмена данными с внешними приложениями через OLE-интерфейс; возможность непосредственного ввода трехмерных данных с помощью координатно-измерительного манипулятора; наличие бесплатного «просмотрщика» (PowerSHAPE Viewer) для ранее созданных моделей и т.д. В перспективе рассматривается проект выпуска компьютерного атласа шеи, легких и верхнего этажа брюшной полости на CD-диске.
СЕРДЦЕ / ОБРАТНАЯ ЗАДАЧА ЭЛЕКТРОКАРДИОГРАФИИ / ЭЛЕКТРИЧЕСКАЯ АКТИВНОСТЬ СЕРДЦА / ТРЕХМЕРНАЯ МОДЕЛЬ / ВИЗУАЛИЗАЦИЯ / HEART / INVERSE PROBLEM OF ELECTROCARDIOGRAPHY / ELECTRICAL ACTIVITY OF THE HEART / 3D MODEL / VISUALIZATION
SIMULATION AND VISUALIZATION OF HEART WORK IN COMPUTER APPLICATIONS
One of up-to-date directions of interactive computer systems development is simulation and visualization of dynamic objects, particularly of human organs. These applications are diagnostic systems, simulation training, monitoring etc. One of important tasks of these systems development is simulation and visualization of heart work. There is no universal software that realizes these functions nowadays. The author scrutinizes the tasks of simulation and visualization of heart work in computer applications, defines the requirements. The generalized algorithm of resolving these tasks is proposed. It consists of steps of heart electrical activity (HEA) determination on the base of registered electrocardiosignal (ECS), myocardium contractions mechanical parameters determination, transformation of 3D model of the heart computation and visualization . The architecture of the system of simulation and visualization of heart work for computer applications is designed in the article.
Текст научной работы на тему «Моделирование и визуализация работы сердца в компьютерных приложениях»
МОДЕЛИРОВАНИЕ И ВИЗУАЛИЗАЦИЯ РАБОТЫ СЕРДЦА В КОМПЬЮТЕРНЫХ ПРИЛОЖЕНИЯХ
© 2015 А. В. Кузьмин
Пензенский государственный университет
Поступила в редакцию 30.07.2015
Ключевые слова: сердце; обратная задача электрокардиографии; электрическая активность сердца; трехмерная модель, визуализация.
Сердце человека представляет собой сложную систему, его рассмотрением с различных сточек зрения занимаются различные науки. В настоящее время уровень развития информационных технологий позволяет строить развитые многоуровневые интерфейсы систем, решающих прикладные задачи. Задача отображения состояния сердца, его электрической и сократительной активности актуальна в следующих прикладных разработках:
- медицинские системы учебного назначения (хирургические тренажеры, интерактивные атласы и др.);
- другие приложения (игры и др.)
В приведенных выше разработках важным аспектом повышения эффективности представления данных и расширения функциональных возможностей является визуализация сокращений сердца на основе электрокардиосигналов (ЭКС).
Набор задач, которые должна решать система моделирования и визуализации в составе комплекса, можно рассмотреть на примере хирургического тренажера [1].
Одним из развиваемых в настоящее время направлений медицинского тренажеростроения является разработка комплексов для эндова-скулярной хирургии. Они представляют собой сложные аппаратно-программные системы, позволяющие пользователю отрабатывать технику
проведения операций. При этом проведение операции моделируется с помощью компьютера, визуальная информация об информационном поле представляется на экране компьютера, а роль хирургических инструментов выполняют их точные копии, подключенные к датчикам, контролирующим перемещения и специальным приводам, имитирующим сопротивление тканей и органов, что позволяет отрабатывать технику владения инструментами в условиях, приближенных к реальным.
При проведении такой виртуальной операции важно с высокой степенью реалистичности имитировать работу сердца пациента. В архитектуре хирургического тренажера [2] предусмотрена реализация следующих задач:
- отображение ЭКС (воспроизводит монитор пациента во время операции, где в реальном масштабе времени отображаются ЭКС, частота сердечных сокращений и давление);
- имитация действия медикаментов (воспроизводит действие на сердечно - сосудистую систему пациента введенных лекарств);
- воспроизведение сердцебиений (имитирует сердечные сокращения, которые врач наблюдает на виртуальном операционном поле).
Но решаются поставленные задачи использованием заранее подготовленных образцов ЭКС и потенциальных реакций на медикаменты и анимированными фрагментами на основе видеозаписей реальных рентгенограмм. Такое решение нельзя считать удовлетворительным, поскольку диапазон возможных состояний сердца пациента ограничен фиксированным набором заранее подготовленных данных (ЭКС и аними-
Известия Самарского научного центра Российской академии наук, т.17, №2(5), 2015
рованных фрагментов работы сердца). Кроме того достоверность визуализации сокращений сердца и соответствие записанных фрагментов ЭКС этим сокращениям может быть обеспечена только путем записи данных в условиях реальных операций, что крайне затруднительно и затратно.
Таким образом, можно сформулировать требования к системе моделирования и визуализации работы сердца:
- воспроизведение основных геометрических параметров модели сердца виртуального пациента;
- возможность работы в реальном масштабе времени;
- наличие критерия достоверности модели.
Решение данной задачи состоит в моделировании сокращений сердца с использованием динамической трехмерной модели.
Работа сердца рассматривается как сложный биомеханический процесс, в основе которого лежат две взаимосвязанные составляющие: электрическая и механическая. Обе эти составляющие на протяжении многих лет являются предметом изучения различных наук (биофизики, биомеханики, медицины, физиологии, математического моделирования, химии, кибернетики и др.). Однако модели, разработанные в рамках этих наук, зачастую воспроизводят определенные аспекты работы сердца достаточно подробно, но крайне сложны для реализации в комплексе и учитывают много факторов, которыми для решения поставленной задачи можно пренебречь. Сдерживающим фактором здесь является сложность реализации имеющихся моделей, вычислительные затраты, возможные погрешности моделирования. В то же время, если в решаемых задачах допускается определенный уровень погрешностей, то возможно использование упрощенных моделей, воспроизводящих основные зависимости и позволяющих осуществить следующие действия: ЭКС - обратная задача электрокардиографии -параметры модели электрической активности сердца (ЭАС) - параметры модели сократительной активности миокарда - визуализация.
Электрическая составляющая работы сердца обусловлена перемещением заряженных ионов через клеточную мембрану (изменением трансмембранных потенциалов). В свою очередь, механическая составляющая обусловлена сокращением мышечных волокон, сопровождающимся кальциевыми токами в клетках мышц миокарда [3]. Данные процессы составляют электрическую активность сердца (ЭАС) и фиксируются на ЭКС.
Большинство математических моделей, описывающих электрические и сократительные процессы, протекающие в клетках миокарда, построено в семидесятых - восьмидесятых годах
прошлого века, в том числе, и силами отечественных биофизиков [3, 4, 5]. Экспериментально установлены временные, силовые и электрические параметры сокращений мышечных волокон [6, 7].
В свою очередь, моделирование работы сердца как электрического генератора - источника ЭКС, т.е. эквивалентного электрического генератора сердца (ЭЭГС) также является достаточно проработанной задачей. Предложен ряд соответствующих моделей, представляющих сердце в виде набора электрически активных элементов. Согласно многодипольной модели [8] сердце состоит из конечного числа диполей, фиксированных в определенных точках миокарда, что позволяет использовать данную модель для получения более детальной информации о состоянии сердца. При этом тело человека рассматривается как изотропная и однородная среда с усредненным удельным сопротивлением. Поверхность грудной клетки моделируется эллиптическим цилиндром.
Характеристиками многодипольного ЭЭГС являются значения дипольных моментов D. модели сердца, вычисленные по потенциалам ц>. в точках стандартных отведений в течение одного кардиоцикла в ходе решения обратной задачи электрокардиографии: р ' cosa,
где 9;.(í) - суммарный поверхностный потенциал в точке измерения j [В];
р - среднее удельное сопротивление тела [Ом*м];
a.. - угол между вектором дипольного момента D; и прямой, соединяющей j-ю точку отведения с каждым диполем сердца;
г.. - расстояние от диполей модели сердца до точек отведений [м];
D¡.(t)-дипольный момент г-го диполя модели сердца (г = 1. I) [А*м];
I - количество диполей модели сердца;
N - количество отведений.
Использование многодипольной модели ЭЭГС позволяет работать с трехмерной моделью сердца сложной геометрической формы, построенной на основе опорных точек. При этом геометрическое место точек - элементарных генераторов, направления векторов дипольных моментов D¡ напрямую влияют на результаты моделирования.
Определение электрических параметров заключается в определении численных характеристик элементарных электрически активных элементов ЭЭГС на основе заданного ЭКС и геометрических характеристик модели сердца.
Рис. 1. Обобщенный алгоритм моделирования и визуализации сокращений сердца
Предполагает решение обратной задачи электрокардиографии с определенными допущениями. Такими как:
- отсутствие влияния внутренних электрических неоднородностей тела, упрощение и усреднение принятой геометрической модели тела,
- направления составляющих диполей определяются заранее и при решении обратной задачи считаются известными и совпадают с направ-
лением нормали к данной точке геометрической модели сердца.
Определение параметров сокращения состоит в определении механических характеристик сокращения для каждой точки поверхности модели сердца в данный момент времени с учетом известных электрических параметров. При этом зависимость в некоторых случаях может быть просто интерполирована на основе имеющихся экспериментальных данных, т.к. модели подробные модели сокращений имеют дело с отдельными мышечными волокнами [5], что ведет к значительным вычислительным затратам.
На этапе определения параметров трансформации определяется направление и величина смещения каждой опорной точки поверхностной модели сердца. В качестве направления предлагается использовать направление нормали, как показано на рис. 2. Величина смещения в каждой фазе сокращения зависит от рассчитанных механических параметров сокращения для каждой опорной точки.
Визуализация сокращений сердца производится средствами компьютерной графики с использованием трехмерной полигональной (каркасной) модели сердца.
Предложенная архитектура системы моделирования и визуализации работы сердца приведена на рис. 3.
Рис. 2. Динамическое изменение положения опорной точки каркаса
Известия Самарского научного центра Российской академии наук, т.17, №2(5), 2015
Рис. 3. Архитектура системы
Основные элементы предложенной архитектуры (см. рис. 3):
- модуль программного интерфейса (API) позволяет внешней программе взаимодействовать с системой, активировать требуемые функции;
- подсистема обработки входных данных позволяет получать и обрабатывать исходные данные из внешних источников (файлов, БД и др.);
- подсистема моделирования выполняет основную функцию системы - моделирование ЭАС с использованием геометрических параметров модели сердца [6] и расчет на основе параметров ЭАС параметров механических сокращений;
- модуль расчета характеристик гемодинамики позволяет косвенно оценить кровоток на основе данных сократительной активности;
- модуль цветового кодирования необходим визуализации механических и электрических параметров на поверхности модели сердца.
Статья подготовлена при выполнении НИР № 1034 в рамках базовой части государственного задания в сфере научной деятельности по Заданию № 2014/151 за 2014 год по теме: «Моделирование электрической активности сердца».
1. Комплекс «Виртуальный хирург» для симуляцион-ного обучения хирургии / А.В. Колсанов, А.В. Ива-щенко, А.В. Кузьмин, А. С. Черепанов // Медицинская техника. 2013. №6. C. 7-10.
2. Architecture of Software development kit for Surgery training suites / A. Kolsanov, A. Nazaryan, A. Ivaschenko, A. Kuzmin // International Journal of Applied Engineering Research. 2014. Vol. 9. №24. P. 25645 - 25652.
3. Дещеревский В.И. Математические модели мышечного сокращения [под ред. акад. Г.М. Франка]. М.: Наука, 1977. 160 с.
4. Моделирование электрической активности сердца // Биофизика сложных систем и радиационных нарушений [под ред. акад. Г.М. Франка]. М.: Наука, 1977. С. 119-129.
5. Типанс И.О. Математическое моделирование процессов возбуждения и сокращения в клетках сердца: дисс. . канд. физ-мат.. наук: 03.00.02. Рига, 1984. 169 с.
6. Brutsaert D.L. Housmans P.R. Load clamp analysis of maximal force potential of mammalian cardiac muscle // The Journal of Physiology. 1977. Vol. 271. Issue 3. P. 587-603.
7. The Effects of Shortening on Myoplasmic Calcium
Concentration and on the Action Potential in Mammalian Ventricular Muscle / M.J. Lab, D. G. Allen, C.H. Orchard // Circulation Research. 1984. Vol. 55, №6. P.825-829. 8. Титомир Л.И., Кнеппо П. Математическое моделирование биоэлектрического генератора сердца. М.:
SIMULATION AND VISUALIZATION OF HEART WORK IN COMPUTER APPLICATIONS
© 2015 A.V. Kuzmin Penza State University
One of up-to-date directions of interactive computer systems development is simulation and visualization of dynamic objects, particularly of human organs. These applications are diagnostic systems, simulation training, monitoring etc. One of important tasks of these systems development is simulation and visualization of heart work. There is no universal software that realizes these functions nowadays. The author scrutinizes the tasks of simulation and visualization of heart work in computer applications, defines the requirements. The generalized algorithm of resolving these tasks is proposed. It consists of steps of heart electrical activity (HEA) determination on the base of registered electrocardiosignal (ECS), myocardium contractions mechanical parameters determination, transformation of 3D model of the heart computation and visualization. The architecture of the system of simulation and visualization of heart work for computer applications is designed in the article.
Keywords: heart; inverse problem of electrocardiography; electrical activity of the heart; 3D model, visualization.
Аннотация научной статьи по математике, автор научной работы — Рущенко Н.Г., Тозик В.Т., Меженин А.В.
В статье рассматриваются вопросы получения трехмерных моделей органов человека на основе томографических данных. Обсуждается один из методов вычисление Фурье-образа проекций.
Похожие темы научных работ по компьютерным и информационным наукам , автор научной работы — Кузьмин Андрей Викторович
Определение дипольных моментов при моделировании электрической активности сердца с модификацией геометрических параметров
Исследование влияния геометрических параметров модели на ошибку определения параметров электрической активности сердца
Аннотация научной статьи по компьютерным и информационным наукам, автор научной работы — Кузьмин Андрей Викторович
Что нужно знать, направляясь на компьютерную томографию
Чтобы пройти МСКТ, необходимо направление от врача, в котором бы указывались область и цель исследования. При направлении на МСКТ с болюсным контрастированием также необходимо иметь на руках заключение аллерголога с разрешением на проведение исследования или рекомендациями о предварительной подготовке. Если у Вас на руках нет направления, Вы можете обратиться в любую из поликлиник «Семейного доктора», записавшись на прием к врачу-специалисту или врачу общей практики. Вас осмотрит опытный специалист, даст свои рекомендации и выпишет направление на МСКТ.
В зависимости от области исследования, Вам может потребоваться подготовка к прохождению МСКТ. Например, МСКТ печени и желчного пузыря делаются утром строго натощак. МСКТ почек или органов малого таза можно делать в течение дня, при этом допустим легкий завтрак. МСКТ головного мозга, носовых пазух, органов грудной клетки, костей и суставов можно делать в любое время, так как специальной подготовки к данным исследованиям не требуется.
Для более точного, индивидуального подбора программы проведения МСКТ и прицельной реконструкции изображений желательно иметь при себе все медицинские документы, отражающие историю заболевания. Возьмите с собой все имеющиеся у Вас результаты прошлых исследований (рентген, УЗИ, УЗЛГ, КТ, МРТ, ПЭТ). Весь ваш архив будет вам полностью возвращен вместе с результатами МСКТ.
Во время прохождения исследования Вам потребуется по указанию врача сохранять неподвижное положение и задержать дыхание на 10-20 секунд.
Может ли компьютерное моделирование помочь в решении проблем людей, страдающих сердечно-сосудистыми заболеваниями? Ученые из Университета ИТМО совместно с коллегами из Нидерландов и Великобритании на протяжении последних нескольких лет ведут исследования, цель которых — сократить риск осложнений после установки пациентам стента — специального распирающего каркаса, который помещается в коронарные сосуды и призван восстановить кровоснабжение сердца. Последний месяц один из авторов проекта, аспирант кафедры высокопроизводительных вычислений Университета ИТМО Павел Зун провел в Университете Шеффилда, где продолжал работу по построению модели роста ткани внутри сосуда после установки в нем стента и выстраивал совместную работу с учеными-биологами. О деталях совместной работы и о том, почему сегодня построение компьютерных моделей для медицины является одной из самых перспективных областей, он рассказал ITMO.NEWS.

Чтобы полностью обеспечить ткани и органы всеми необходимыми веществами и кислородом, нужна не только разветвленная сеть артерий, которые эту доставку к сердцу и обеспечивают, но и ее правильная работа. Коронарные артерии снабжают ткани самого сердца. Патологические изменения в этих артериях ведут к ухудшению работы системы кровоснабжения сердца. Следствием таких изменений и нарушений становятся различные сердечно-сосудистые заболевания, в первую очередь ишемия и острый коронарный синдром. Эти заболевания и сопутствующие повреждения сердечной мышцы — миокарда — обычно бывают вызваны патологическим сужением коронарных сосудов.
Долгое время для лечения суженных участков коронарных сосудов было применимо только хирургическое вмешательство со вскрытием грудной клетки. Однако в последние десятилетия появились и начали широко использоваться менее травматичные методы, позволяющие получить доступ к суженному сосуду, введя катетер в артерию. Одним из них является коронарное стентирование сосудов.
Стентирование коронарных артерий является одной из наиболее безопасных и эффективных процедур восстановления нормального просвета артерий, имеющих атеросклеротические изменения. Стент представляет собой сетчатый цилиндрический металлический каркас, разворачиваемый в закупоренном участке артерии и удерживающий ее от повторного сужения. После установки стент естественным образом покрывается тканью внутренней выстилки сосуда.
Однако установка стента не всегда проходит успешно, в некоторых случаях развивается рестеноз — осложнение, которое характеризуется чрезмерным разрастанием ткани и повторным сужением просвета артерии. На сегодняшний день причины рестеноза изучаются, ведутся исследования по оптимизации конфигурации стента и процедуры лечения для снижения частоты осложнений.
Как в этом может помочь компьютерное моделирование?
Одним из способов в определении причин развития рестеноза является проведение опытов с использованием клеточных культур и модельных животных. Подобные исследования, например, ведутся в Университете Шеффилда. Однако в понимании причин развития рестеноза, а также впоследствии разработке более эффективного дизайна стента, который позволит снизить процент осложнений, может помочь и компьютерное моделирование.
Соответствующими исследованиями занимаются специалисты Института наукоемких компьютерных технологий Университета ИТМО, которые совместно с коллегами из Амстердамского университета в Нидерландах и Университета Шеффилда в Великобритании, последние несколько лет работают над построением модели нежелательного роста ткани внутри сосуда после установки в нем стента — распирающего каркаса.
Модель может помочь понять, почему в некоторых случаях ткани слишком интенсивно прорастают сквозь стент и сосуд повторно сужается, то есть происходит рестеноз, поясняет Павел Зун, аспирант кафедры высокопроизводительных вычислений Университета ИТМО. Воспроизводя этот процесс, ученые научились моделировать клеточный рост артериальной стенки, физические взаимодействия, возникающие из-за того, что стент растягивает сосуд, а также то, как лекарственные вещества со стента проникают вглубь тканей.
В рамках проекта последний месяц Павел Зун провел в Университете Шеффилда, где работал над дальнейшим улучшением модели и валидацией результатов, полученных в ходе компьютерного моделирования.
«Процесс разработки модели выглядит следующим образом: сначала ученые ставят эксперименты. Например, они берут клетки и высаживают их в чашки Петри, а затем смотрят, как эти клетки ведут себя под воздействием течений, как они мигрируют и так далее. На основе данных, которые получены из большого количества экспериментов, строится гипотеза о том, какие механизмы влияют на поведение клеток. А, в свою очередь, на основе этой гипотезы строится модель: мы устанавливаем определенные правила поведения клеток в модели в зависимости от того, что мы хотим проверить. После этого мы проверяем, насколько поведение клеток в модели с определенным набором правил соответствует тому, что происходит в реальности, — рассказывает Павел Зун. — Таким образом, моя работа в Шеффилде заключалась в поиске экспериментальных данных, а также в выстраивании сотрудничества с учеными-биологами. Ведь мы можем построить модель, а они могут поставить соответствующие эксперименты in vitro, на клеточных культурах, или на животных, in vivo. В дальнейшем эти эксперименты могут быть использованы для валидации и подтверждения наших моделей».
Одним из основных факторов, вызывающих остановку роста ткани в сосуде, является восстановление клеток внутренней выстилки сосуда — эндотелия. Таким образом, чтобы описывать процессы, происходящие в сосуде, необходимо знать, в том числе как происходит миграция клеток эндотелия после установки стента и, соответственно, проходит процесс заживления. Это можно изучить, высадив эти клетки в экспериментальную установку, имитирующую стентированный участок сосуда, и поняв, как они будут перемещаться там под действием течений, добавляет он. Изучая эти процессы, можно получить траектории движения клеток, что и реализуют исследователи при построении компьютерных моделей. И, как отмечает Павел Зун, за последнее время ученым удалось добиться достаточно неплохой точности модели.

Компьютерная модель
«Например, с помощью моделирования мы видим, что между помещенными на поверхность установки ребрами, имитирующими элементы стента, возникают завихрения текущей сквозь установку жидкости. Это влияет на траектории миграции клеток, и мы можем высказать предположение, почему это происходит, — объясняет исследователь. — Соответственно, на основе моделирования мы можем предложить новый дизайн эксперимента, чтобы проверить это предположение. Если это предположение будет корректным, это повлияет на дизайн стентов, что в будущем позволит уменьшить риск осложнений после операций».
Риск осложнений после установки первых стентов, которые начали применяться в 90-х годах прошлого века, достигал 20%. Современные устройства помогли свести этот показатель до пяти случаев из ста. Однако, учитывая, что стентирование коронарных сосудов является одной из самых распространенных операций в современной медицинской практике, дальнейшее улучшение дизайна стентов и сокращение риска осложнений и сегодня является актуальной задачей для исследователей, говорит Павел Зун.
Сегодня ученые продолжают работать над улучшением модели. В ближайшей перспективе исследователи собираются проверить еще одну гипотезу, согласно которой на ускорение заживления артерии после стентирования может повлиять покрытие стента специальным веществом, подавляющим Rho-ассоциированную протеинкиназу в клетках (ROCK), отвечающую за реакцию клеток на локальное направление течения крови. Этот механизм ученые также реализуют в модели и по итогам работы проверят, насколько она будет соответствовать экспериментальным исследованиям.
Перспективы
Построение модели роста ткани внутри сосуда после установки в нем стента является частью работы, которую в последние несколько лет проводят ученые из Амстердама и Петербурга. Ранее в исследовании, опубликованном в журнале Philosophical Transactions A, они представили концепцию «виртуальной артерии», показав, что эта мультимасштабная компьютерная модель объединит в себе несколько подмоделей, описывающих участки сердечно-сосудистой системы в разном приближении. Разработчики считают, что детальная имитация человеческой артерии позволит глубже изучить заболевания сосудов и создаст альтернативу испытаниям лекарств на животных.
Полноценная виртуальная артерия, по мнению ученых, позволит изучать более широкий спектр сердечно-сосудистых заболеваний, совместив в себе несколько разноуровневых моделей. На первом уровне разработчики воспроизводят кровоток по всему телу. Углубляясь, они переходят к трехмерному участку кровеносного сосуда. На самом низком уровне рассматриваются взаимодействия между клетками внутри артериальной стенки. Таким образом, шаг за шагом ученые подходят к более точному воспроизведению сложных природных процессов.
Сейчас ученые Университета ИТМО продолжают сотрудничество с научной группой Амстердамского университета, а также со специалистами Университета Шеффилда. Кроме того, недавно было налажено сотрудничество с исследователями Политехнического университета Милана, которые также занимаются моделированием течений в стентированных сосудах, рассказывает Павел Зун.
По его словам, сегодня построение компьютерных моделей для медицины является одной из интересных и перспективных задач. Именно в этой области в последнее время появляется большое количество новых проектов, в реализации которых могут применить свои силы перспективные магистранты и аспиранты.
«Заниматься моделированием именно в области биохимии, медицины очень интересно, потому что модели в данной области развиты пока не настолько, как, например, в физике или в неорганической химии. Это очень сложные системы, поэтому здесь пока существует непаханное поле для исследований. Да, уже в 90-е были попытки моделирования систем в этой области, но тогда, разумеется, мощность компьютеров не позволяла делать сложные модели, — говорит Павел Зун. — Пока самое главное, чего не хватает в этой области, — это люди. Сейчас такими исследованиями занимаются немного магистрантов и аспирантов. Между тем, сегодня существует очень много проектов по этой тематике, поэтому спрос на квалифицированных специалистов очень большой».
Текст научной работы на тему «Компьютерное моделирование органов человека»
КОМПЬЮТЕРНОЕ МОДЕЛИРОВАНИЕ ОРГАНОВ ЧЕЛОВЕКА Н.Г. Рущенко, В.Т. Тозик, А.В. Меженин
В статье рассматриваются вопросы получения трехмерных моделей органов человека на основе томографических данных. Обсуждается один из методов — вычисление Фурье-образа проекций.
В настоящее время ЗБ-реконструкция внутренних органов человека на основе рентгенографии, ультразвуковых исследований, компьютерной и магнитно-резонансной томография получает все большее распространение и является актуальной задачей. Применение этих современных методов исследования позволяет врачу рассмотреть и оценить состояние органов и организма в целом. При этом, к примеру, при постановке вопроса о хирургической операции врач может реально увидеть оперируемый орган на экране компьютера и оценить объем хирургического вмешательства.
На кафедре ИКГ совместно с научно-исследовательским институтом им. Г.И. Турнера проводятся исследования в этой области.
Рассмотрим этапы получения трехмерных компьютерных моделей.
Первый этап - получение исходной морфометрической информации. Для этого используются клинико-инструментальные методы исследования (рентгенография, ультразвуковое исследование, компьютерная и магнитно-резонансная томография и др.). Полученные в результате проведенного исследования количественные данные используются на втором и третьем этапах для создания компьютерных моделей, имеющих установленные при морфометрии параметры и расположенные в виртуальном пространстве.
Второй этап создания компьютерной модели заключался в построении плоскостной двухмерной модели органа человека в трех проекциях.
Третий этап - трехмерная реконструкция и создание объемной компьютерной модели.
Второй и третий этапы планируется выполнить с использованием специально разработанного программного обеспечения и системы трехмерного моделирования 3ds max [1].
Созданные компьютерные модели могут быть продемонстрированы на дисплее, повернуты в любой плоскости и распечатаны на принтере в виде фотографий. Используя возможности программы 3ds max, можно перемещать компьютерные модели в виртуальном пространстве, что позволяет сдвинуть или удалить отдельные элементы модели для изучения особенностей топографии области. Кроме этого, планируется, используя систему инверсной кинематики, моделировать поведение элементов позвоночника при его лечении.
Трехмерные компьютерные модели могут быть полезны для повышения эффективности рентгенодиагностических методик, при планировании хирургических вмешательств. Кроме этого, возможно их использование как наглядных пособий не только в учебном процессе, но и различных научных исследованиях.
Использование преобразования Фурье для SD-реконструкция объектов
Геометрия исходных данных (2Б-проекций) при исследовании объектов томографическими методами [2] может быть получена расположением зоны 2Б-проекций по образующим к цилиндрической поверхности, на осевой линии которой расположен исследуемый объект. В диаметрально противоположных направлениях позиционируется
источник излучения. Рассмотрим математический аппарат, который может быть использован в этом случае [3].
В каждой проекции регистрируемая интенсивность поля излучения -/(х, у) ^/(г). Для реконструкции в первом приближении выбирается функция в виде
В2 ( х, у ) = | ¡и ( х; у; £ ) dz , здесь (х, у)- двумерная функция проекции, Ь -
толщина объекта в направлении просвечивания, ¡и(х; у; г) - линейный (массовый) коэффициент ослабления по объему контролируемого образца. Если плотности внутренних локальных объектов постоянны, то последнее соотношение можно упростить:
ла изделия, и1- коэффициент ослабления материала локального объекта, I (х; у^) -
размер локального объекта в направлении просвечивания, к - их число в направлении просвечивания. Нормализованные функции проекций -
ё ( Р ) = | / ( г ( Р - гГ) dl , в том числе и одномерные ё (г; в), ё (р), «вычле-
няемые» из двумерных, должны удовлетворять условию
Точность реконструкции формы поверхности в этом варианте определяется точностью восстановления границ сечений, поэтому разработан следующий способ реконструкции сечений и контуров исследуемых объектов.
• Задается формат сечения. Форматы изображений локальных объектов выбираются в пределах (64x64), (256x256) элементов. Требуемое число проекций определяется конечным выбранным форматом изображения. Этот набор ёв (р) дополняется набором ёв+п(Р) . Недостающее количество проекций доопределяется, методами интерполяции.
• Для данного сечения вычисляются Фурье-образы проекций при числе отсчетов в каждой проекции, в несколько (3-6) раз превышающих линейный формат матрицы изображения сечения. В соответствии с теоремой о сечениях формируется «двумерный Фурье-спектр».
• По кольцевым гармоникам производится интерполяции в зонах отсутствия отсчетов. Так как спектры реальных проекций содержат дополнительные отсчеты, то процедуру интерполяции можно оптимизировать, используя зоны дополнительных отсчетов, и таким образом оптимизировать двумерный спектр Фурье - «выгладить» его.
• Наборы одномерных спектров проекций пересчитываются в функции проекций, оптимизируется ядро алгоритма свертки. Для данного класса задач ядро оказывается достаточно «низкочастотным», в общем случае его Фурье-образ в области главного максимума имеет вид
^ Л а(2п)2е"2с еов(с2)вт(с2)
здесь а - константа, выбираемая в пределах (0,9-2,4).
• После нормализации всех функций проекций (реальных и вычисленных) для данного сечения производится реконструкция каждого сечения с помощью стандартной
процедуры - сверточного алгоритма, включающего вычисление одномерных сверток проекций с выбранным ядром и процедуру обратного проецирования. Таким образом, формируется заданное количество сечений, при этом все вычислительные процедуры реализуют только одномерные преобразования: вычисление прямых, обратных преобразований Фурье от функций проекций, интерполяция по кольцевым гармоникам в двумерном Фурье спектре, операция свертки. Это сокращает время реконструкции, алгоритмы могут быть реализованы на стандартных ПК. В то же время фактически оказывается вычисленным ЭБ-массив, определяющий конфигурацию локального объекта и его ориентацию в пространстве.
Рассмотренный математический аппарат положен в основу разрабатываемого программного обеспечения, которое в настоящее время находится в стадии отладки.
1. ЭёБ Мах 9: трехмерное моделирование и анимация / В.Т. Тозик, А.В. Меженин. -СПб.: БХВ-Петербург, 2007. 1056 с.: ил.
2. Рущенко Н.Г. Исследование и разработка методов решения задачи синтеза высокооднородного магнитного поля в МР- томографе. Автореферат дисс. канд.техн.наук -СПб: ИТМО,2004.
3. Филонин О.В., Шадрунов А. А. Цифровые методы обработки в компьютерной томографии / Тр. межд. симп. «Надежность и качество». Пенза, 2004. С. 257-261.
Компьютерная томография (КТ) – это метод диагностики, основанный на послойном исследовании структуры внутренних органов и систем; данные получаются с помощью рентгенологического оборудования, совмещенного с мощной компьютерной станцией, позволяющей проводить оперативный детальный анализ изображения.
Преимущества компьютерной томографии (МСКТ) как метода диагностики
Компьютерная томография является одним из лучших неинвазивных (осуществляемых без повреждения тканей) диагностических методов. Высокая разрешающая способность МСКТ в сочетании с передовым программным обеспечением, позволяющим реконструировать очень тонкие срезы, визуализируют изменения, размеры которых не превышают даже нескольких миллиметров, что дает возможность обнаруживать заболевания на самых ранних стадиях.
В некоторых случаях проводится компьютерная томография с болюсным контрастированием. Современные томографы оборудованы встроенным автоматическим инъектором, с помощью которого через специальный катетер в локтевую вену вводится контрастное вещество. Работа инъектора синхронизирована с процессом сканирования. Болюсное контрастирование позволяет оценить характер накопления контрастного вещества, что расширяет возможности диагностики. В качестве контрастного вещества при болюсном контрастировании используются йодсодержащие препараты.
Важными преимуществами компьютерной томографии также являются:
- возможность получения объемных изображений внутренних органов;
- быстрота проведения (само исследование длится менее полминуты, дольше одеваться);
- комфорт (пациент не испытывает неприятных ощущений).
Как устроен томограф
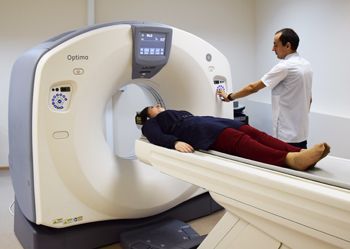
Компьютерная томография
Главная часть любого современного томографа это гентри – кольцо, внутри которого быстро вращается лучевая трубка, напротив которой расположены датчики. Пациент ложится на двигающийся стол, перемещающийся внутри этого кольца. Движение стола и рентгеновской трубки синхронизированы так, чтобы в результате считывание информации осуществлялось по спирали, обходящей тело пациента в области отдела, подлежащего исследованию, со всех сторон. Подобное исследование еще называется мультиспиральной компьютерной томогорафией (МСКТ). Приставка «мульти» означает, что в современных томографах датчики установлены не в один ряд (таких рядов может быть много). Это позволяет не только получать больше информации за один оборот лучевой трубки (что увеличивает скорость обследования и снижает лучевую нагрузку), но и отследить работу динамических органов и структур (сердца, грудной клетки, суставов в движении).
Компьютерная томография в «Семейном докторе»
В «Семейном докторе» используются томографы нового поколения GE OPTIMA CT660 производства GE Healthcare (подразделение корпорации General Electric, США). Данный аппарат делает 64 изображения-среза за один оборот, что значительно ускоряет процесс диагностики. Отличительной особенностью аппарата является его высокая разрешающая способность, позволяющая создавать качественную двухмерную (2D) и трехмерную (3D) реконструкцию изображений.
Другие преимущества GE OPTIMA CT660:
- улучшенная эргономика сканера, обеспечивающая пациенту максимальный комфорт;
- настройка параметров сканирования осуществляется в присутствии пациента, таки образом у него есть время, чтобы освоиться;
- диагностика проводится буквально за секунды, при этом доза облучения оптимизируется, чтобы обеспечить минимально возможную лучевую нагрузку.
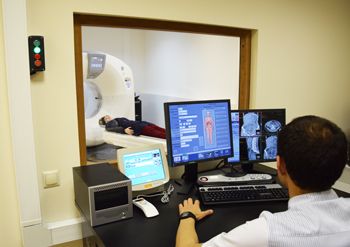
МСКТ-исследование
Поликлиники, в которых оказываются услуги компьютерной томографии, можно посмотреть по ссылке>>>
Похожие темы научных работ по математике , автор научной работы — Рущенко Н.Г., Тозик В.Т., Меженин А.В.
Исследование возможностей малоракурсной томографической прямой 3D реконструкции параметров индуцированных оптоэлектронных полей излучения непрозрачных объектов
Методы и средства оптико рентгеновской 3D диагностики процессов сублимации в композиционных материалах
Система трехмерной томографической диагностики параметров плазменных образований в условиях ближнего космоса
Методы и средства малоракурсной томографической диагностики параметров потоков ионных и плазменных двигателей КЛА
Что исследуется с помощью МСКТ (мультиспиральной компьютерной томографии)?
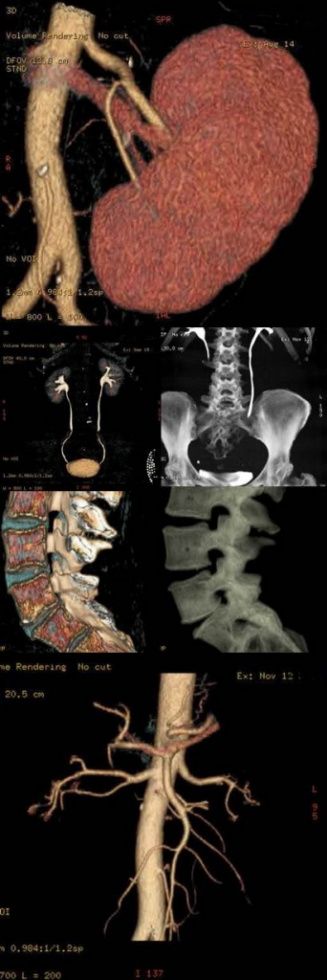
Компьютерные реконструкции
Мультиспиральная компьютерная томография используется для исследования следующих органов и областей организма:
- головной мозг. МСКТ головного мозга позволяет выявлять различные заболевания серого и белого вещества мозга, а также нарушения со стороны окружающих тканей, оболочек и сосудов. Могут быть выявлены аномалии развития, воспалительные очаги, доброкачественные и злокачественные новообразования, сосудистые расстройства, кровоизлияния, гематомы, геморрагические и ишемические инсульты;
- кости черепа. Востребованными исследованиями являются МСКТ лицевого отдела черепа и МСКТ височных костей, которая проводится с высокой детализацией костной ткани; . Реконструкция в двух и более проекциях дает возможность обнаружить причины заложенности носа и снижения обоняния, определить наличие гноя в пазухах, выявить полипы и дефекты носовых ходов. В рамках одного исследования может проводиться МСКТ пазух носа и височных костей.
- органы грудной клетки. МСКТ органов грудной клетки позволяет исследовать легкие, плевру, трахею и бронхи, органы средостения: пищевод, сердце, аорту, лимфатические узлы, молочные железы. С помощью МСКТ могут быть выявлены туберкулез, пневмония, доброкачественные и раковые опухоли различной локализации, аномалии развития, посттравматические изменения, сосудистые нарушения и другие заболевания;
- позвоночник. МСКТ позвоночника – более информативное исследование, чем обычная рентгенография. Оно позволяет получить объемную картину, увидеть позвоночник в различных проекциях, что расширяет возможности диагностики состояния межпозвоночных дисков, повреждений тел позвонков и отростков, состояния позвоночного столба.
- органы брюшной полости и забрюшинного пространства. МСКТ брюшной полости и забрюшинного пространства позволяет визуализировать мягкие ткани этой области. Исследуются печень, желчный пузырь, желчевыводящие пути, поджелудочная железа, селезенка, толстый и тонкий кишечник, почки, надпочечники, мочеточники, а также лимфоузлы и сосуды. Исследование позволяет оценить размер и положение органа, обнаружить патологические образования и диффузные изменения (очаг воспаления, абсцесс и т.п.). Если локализация проблем известна, проводится МСКТ конкретного органа – печени, желчного пузыря и поджелудочной железы; почек и надпочечников; или только надпочечников;
- кишечник. МСКТ позволяет проводить исследование кишечника с созданием объемной (3D) реконструкции изображения органа;
- органы малого таза. При МСКТ органов малого таза обследуются тазовые кости, мочевой пузырь, у женщин - матка и яичники, у мужчин - предстательная железа и семенные пузырьки;
- суставы. МСКТ суставов позволяет обнаружить патологические процессы, происходящие в костях и мягких тканях, составляющих сустав. Чаще всего исследуются тазобедренный и коленный суставы;
- сосуды. МСКТ дает возможность оценить состояние сосудов диаметром от 1 мм. Обследуются сосуды различных областей - головного мозга, шеи, нижних конечностей, аорта и подвздошные артерии;
- глазные орбиты. МСКТ глазных орбит позволяет выявить структурные нарушения глазного яблока, костной основы глазницы, глазодвигательных мышц, глазного нерва, слезных желез.
Читайте также:


