Чем отличается 1с орбиталь от 2с орбитали
Для описания положения электрона в электронной оболочке используют четыре квантовых числа. Здесь мы не будем углубляться в квантово-механические подробности и опишем только утилитарный смысл данных чисел. Набор, состоящий из четырёх квантовых чисел - это «адрес» электрона в электронной оболочке.
Главное квантовое число `n` - определяет полную энергию электрона на энергетическом уровне и показывает, из скольких энергетических уровней состоит электронная оболочка атома. Принимает целочисленные положительные значения от `1` до `oo`. В периодической таблице Д. И. Менделеева `n` равно номеру периода.
Орбитальное квантовое число `l` показывает, сколько энергетических подуровней составляют данный уровень и характеризует форму орбиталей. Принимает значения от `0` до `(n-1)`.
При `n=1`, `l` принимает только одно значение `0` (этому числовому значению соответствует буквенное `s`), следовательно, на первом энергетическом уровне только один подуровень - `s`. Орбиталь `s`-подуровня имеет сферическую форму (рис. 1).
При `n=2`, `l` принимает два значения: `0` `(s)` и `1` `(p)`. Энергетический уровень состоит из двух подуровней - `s` и `p`. Форма `p`-орбитали похожа на объёмную восьмёрку (рис. 1).
При `n=3`, `l` принимает уже три значения: `0` `(s)`; `1` `(p)` и `2` `(d)`. Таким образом, на третьем уровне три подуровня. Орбитали `d`-подуровня имеют форму двух перекрещённых объёмных восьмёрок либо объёмной восьмерки с перемычкой (рис. 1).
При `n=4`, значений `l` уже четыре, следовательно, и подуровней на четвёртом уровне четыре. К перечисленным выше добавляется `3` `(f)`. Орбитали `f`-подуровня имеют более сложную, объёмную, форму.
Магнитное квантовое число `ml` определяет число орбиталей на каждом подуровне и характеризует их взаимное расположение.
Принимает значения `-l` до `+l`, включая `0`.
При `l=0`, `m_l` принимает только одно значение - `0`. Следовательно, орбиталь, находящаяся на данном подуровне (`s`-подуровне), только одна. Мы уже знаем, что она имеет форму сферы с центром в начале координат.
При `l=1`, `m_l` принимает три значения: `−1`; `0`; `+1`. Значит, орбиталей на данном подуровне (`p`-подуровне) три. Так как `p`-орбитали представляют из себя объёмные восьмёрки (то есть линейной структуры), располагаются они в пространстве по осям координат, перпендикулярно друг другу (`p_x`, `p_y`, `p_z`).
При `l=2`, `m_l` принимает уже пять значений: `−2`; `−1`; `0`; `+1`; `+2`. То есть на `d`-подуровне располагаются пять орбиталей. Это плоскостные структуры, в пространстве занимают пять положений.
При `l=3`, то есть на `f`-подуровне, орбиталей становится семь, так как `m_l` - принимает семь значений (от `−3` до `+3` через `0`). Орбитали являются более сложными объёмными структурами, и взаимное их расположение еще более сложно.
Спиновое квантовое число `m_s` характеризует собственный момент количества движения электрона и принимает только два значения: `+1//2` и `-1//2`.
Электронная ёмкость подуровня (максимальное количество электронов на подуровне) может быть рассчитана по формуле `2(2l+1)`, а уровня - по формуле `2n^2`.
Всё вышесказанное можно обобщить в Таблице 2.
Таблица 2. Квантовые числа, атомные орбитали и число электронов на подуровнях (для `n<=4`)
Атом состоит из электронов, которые находятся в непрерывном движении в любом направлении вокруг ядра. Поскольку они движутся вокруг ядра, мы не можем определить точное положение этого электрона в данный момент. Мы можем только догадываться о вероятности того, что электрон окажется в положении. Это явление называется Принцип неопределенности Гейзенберга, Согласно этим вероятностям, области, где электрон может быть найден с наибольшей вероятностью, объясняются термином орбитальный. В зависимости от энергий и движений электронов вокруг ядра могут быть разные орбитали. S орбитальная и p орбитальная две такие орбитали. Основное различие между орбиталью и орбиталью в том, что s орбитали имеют сферическую форму, тогда как p орбитали имеют форму гантелей.
Ключевые области покрыты
1. Что такое S Orbital?
- Определение, форма и структурные свойства
2. Что такое P-орбиталь
- Определение, форма и структурные свойства
3. Каковы сходства между S-орбитальным и P-орбитальным
- Краткое описание общих черт
4. В чем разница между S-орбитальной и P-орбитальной
- Сравнение основных различий
Ключевые слова: атом, принцип неопределенности Гейзенберга, орбитали, P-орбиталь, вероятность, S-орбиталь.

Что такое S Orbital
Орбиталь S - это атомная орбиталь, которая имеет сферическую форму. Он имеет самую низкую энергию по сравнению с другими атомными орбиталями. Каждая электронная оболочка имеет по крайней мере одну s-орбиту. Орбиталь S является самой простой атомной орбиталью среди других орбиталей. Одна орбита может содержать максимум два электрона. S орбитали не имеют суборбиталей. Буква «s» обозначает «острый». Таким образом, эта орбита была названа с учетом момента импульса электронов на этой орбите. Поскольку атомные орбитали состоят из определенного энергетического уровня (энергия квантуется), им присваивается квантовое число. С орбиталью присваивается квантовый номер момента импульса атома.

Рисунок 1: Размер s-орбитали увеличивается с увеличением основного квантового числа
Два электрона на орбитали s имеют противоположные спины. S орбитали участвуют в химической связи. Они могут принимать участие в формировании сигма-связей. Но эти орбитали не могут образовывать пи-связи. Сферическая форма говорит нам наиболее вероятную область, где электроны могут быть найдены. S орбитали не имеют угловых узлов. Следовательно, квантовое число углового момента s-орбитали равно 0.
S-орбиталь имеет самую низкую энергию среди всех других орбиталей в той же электронной оболочке. При более высоких электронных оболочках (главное квантовое число = n) s-орбиталь имеет меньшую энергию, чем энергия d-орбиталей в ближайшей нижней оболочке (n-1). Размеры орбитальной сферы увеличиваются с увеличением принципиального квантового числа.
Что такое P Orbital?
P orbital - это атомная орбиталь, имеющая форму гантели. P-орбитали имеют более высокую энергию, чем s-орбитали. Буква «р» обозначает «главный». Она описывает момент импульса электронов на орбитали. Одна орбиталь может содержать максимум 6 электронов. Эти электроны занимают субатомные орбитали. Одна субатомная орбита может содержать не более двух электронов. Следовательно, одна орбиталь имеет три субатомных орбитали. Они называются px, py и pz. В общем, все они называются p-орбиталями.

Рисунок 2: Формы и ориентации трех P-орбиталей
Три суборбитали орбитали p отличаются друг от друга в зависимости от ориентации этих орбиталей в атоме. Однако они похожи по форме. Все эти суборбиталы имеют форму гантелей. Одна особенность орбитали в том, что она состоит из углового узла. Следовательно, квантовое число углового импульса орбитали равно 1.
За исключением электронной оболочки, имеющей главное квантовое число 1, все другие электронные оболочки состоят из p-орбиталей. Размер р-орбиталей увеличивается с увеличением главного квантового числа. Одна орбиталь имеет две доли. Эти лепестки симметричны вдоль своей оси. Эти p-орбитали участвуют в химической связи. Они могут образовывать либо сигма-связи, либо пи-связи. P суборбиталей в горизонтальной ориентации может для сигма-связей. Два других суборбитала связаны с пи-связью.
Сходства между S Orbital и P Orbital
- S-орбитальный и P-орбитальный типы атомных орбиталей.
- Оба термина описывают момент импульса электронов на этой орбите.
- Обе орбитали участвуют в связывании сигмы.
Разница между S-орбитальной и P-орбитальной
Определение
S Orbital: Орбиталь S - это атомная орбиталь, которая имеет сферическую форму.
P Орбитальный: P-орбиталь - это атомная орбиталь, имеющая форму гантели.
Уровень энергии
S Orbital: S орбитали имеют самые низкие энергетические уровни.
P Орбитальный: P-орбитали имеют более высокую энергию, чем s-орбитали.
Угловые узлы
S Orbital: У орбиталей нет угловых узлов.
P Орбитальный: р-орбитали имеют угловые узлы
Максимальное количество электронов
S Orbital: Максимальное количество электронов, которое может удерживать орбиталь, равно 2.
П Орбитальный: Максимальное количество электронов, которое может удержать орбиталь, равно 6.
Суб-орбитали
S Orbital: В s-орбиталях нет суборбиталей.
П Орбитальный: В орбитали есть 3 суборбитали.
Квантовое число углового момента
S Orbital: Квантовое число углового момента s-орбитали равно 0.
П Орбитальный: Квантовое число углового момента p-орбитали равно 1.
Лопасти
S Orbital: На орбиталях нет лепестков.
P Орбитальный: В p-орбиталях есть лепестки.
Заключение
И s-орбитали, и p-орбитали являются атомными. Эти орбитали указывают наиболее вероятную область, где мы можем найти электрон этого атома. Основное различие между s-орбиталью и p-орбиталью состоит в том, что s-орбитали имеют сферическую форму, тогда как p-орбитали имеют форму гантелей.
Рекомендации:
1. Libretexts. «Атомные орбитали». Химия LibreTexts, Libretexts, 3 ноября 2015 г.,
Видео: Разница между 1 и 2 орбитальными | Сравните разницу между похожими терминами
Содержание:
Ключевое отличие - орбитальная 1 с против 2 с
Атом - мельчайшая единица материи. Другими словами, вся материя состоит из атомов. Атом состоит из субатомных частиц, в основном протонов, электронов и нейтронов. Протоны и электроны составляют ядро, которое находится в центре атома. Но электроны расположены на орбиталях (или энергетических уровнях), которые расположены вне ядра атома. Также важно отметить, что орбитали - это гипотетические концепции, которые используются для объяснения наиболее вероятного местоположения атома. Ядро окружают различные орбитали. Также существуют суборбитали, такие как s, p, d, f и т. Д. Суборбиталь s имеет сферическую форму, если рассматривать ее как трехмерную структуру. S-орбиталь имеет наибольшую вероятность найти электрон вокруг ядра. Суборбиталь снова нумеруется как 1, 2, 3 и т.д. в соответствии с уровнями энергии. Ключевое различие между орбитали 1s и 2s - энергия каждой орбитали. Орбиталь 1s имеет меньшую энергию, чем орбиталь 2s.
СОДЕРЖАНИЕ
1. Обзор и основные отличия
2. Что такое 1s Orbital
3. Что такое 2s Orbital
4. Сравнение "бок о бок" - орбитальная 1 с 2 с.
5. Резюме
Что такое 1s Orbital?
1s-орбиталь - это ближайшая к ядру орбиталь. У него самая низкая энергия среди других орбиталей. Это также самая маленькая сферическая форма. Поэтому радиус s-орбитали мал. На s-орбитали может быть только 2 электрона. Электронную конфигурацию можно записать как 1 с 1 , если на s-орбитали находится только один электрон. Но если есть пара электронов, это можно записать как 1с 2 . Затем два электрона на s-орбитали движутся в противоположных направлениях из-за отталкивания, которое возникает из-за одинаковых электрических зарядов двух электронов. Когда есть неспаренный электрон, он называется парамагнитным. Это потому, что он может притягиваться магнитом. Но если орбиталь заполнена и пара электронов присутствует, электроны не могут быть притянуты магнитом; это известно как диамагнитный.
Что такое 2s Orbital?
Орбиталь 2s больше орбитали 1s. Следовательно, его радиус больше, чем у орбитали 1s. Это следующая закрытая орбиталь ядра после орбитали за 1 с. Его энергия выше орбитали 1 с, но ниже, чем у других орбиталей в атоме. 2s-орбиталь также может быть заполнена одним или двумя электронами. Но 2s-орбиталь заполняется электронами только после завершения 1s-орбитали. Это называется принципом Ауфбау, который указывает порядок заполнения электронами суборбиталей.
В чем разница между 1s и 2s Orbital?
1 с против 2 с орбитальный
Резюме - 1 с против 2 с орбитальной
Атом - это трехмерная структура, содержащая ядро в центре, окруженное орбиталями различной формы с разными уровнями энергии. Эти орбитали снова делятся на подорбитали в соответствии с небольшими различиями в энергии. Электроны, которые являются основной субатомной частицей атома, находятся на этих энергетических уровнях. Суборбитали 1s и 2s находятся ближе всего к ядру. Основное различие между 1s и 2s орбиталями заключается в разнице их энергетических уровней, то есть 2s орбиталь является более высоким уровнем энергии, чем 1s орбиталь.
Ссылка:
1. Либретексты. «Атомные орбитали». Химия LibreTexts. Libretexts, 3 ноября 2015 г. Web. 26 мая 2017. .
2. Атомы, электроны и орбитали. N.p., n.d. Интернет. 26 мая 2017. .
Изображение предоставлено:
1. «S-орбитали» (обрезано) Фондом CK-12 - Файл: High School Chemistry.pdf, стр. 265 (CC BY-SA 3.0) через Commons Wikimedia
Каждый атом состоит из ядра, состоящего из протонов и нейтронов, которые окружены электронами. Эти электроны находятся в постоянном движении вокруг ядра. Поэтому мы не можем дать конкретное местоположение для электрона в атоме. Вместо определения точного положения электрона ученые ввели понятие «вероятность». Другими словами, определяется наиболее вероятный путь, по которому электрон, скорее всего, движется. Этот путь называется орбитальным. Эти орбитали расположены в соответствии с количеством энергии, из которой состоят электроны на этих орбиталях. Это так называемые энергетические уровни. Основное различие между орбиталями и уровнями энергии состоит в том, что орбитали показывают наиболее вероятный путь движения электрона вокруг ядра, тогда как энергетические уровни показывают относительное расположение орбиталей в соответствии с количеством энергии, которой они обладают.
Ключевые области покрыты
1. Что такое орбитали
- Формирование, свойства и расположение
2. Что такое уровни энергии
- Формирование, свойства и расположение
3. Какова связь между орбиталями и уровнями энергии
- орбитали и уровни энергии
4. В чем разница между орбиталями и уровнями энергии
- Сравнение основных различий
Ключевые слова: атом, d орбиталь, электрон, уровни энергии, орбитали, вероятность, p орбиталь, s орбиталь

Какие орбитали
Орбиталь может быть определена как наиболее вероятная область, где электрон может быть найден вокруг ядра. На атомном уровне наиболее точное название орбиты - атомная орбита. Атомная орбита может существовать в нескольких формах, таких как сферическая форма и форма гантели. Орбиталь указывает на наиболее вероятный путь электрона, который движется вокруг ядра атома.
Есть несколько типов орбиталей, которые можно найти вокруг ядра. Немногие из них описаны ниже.
с орбитальной
Это орбитали сферической формы. На том же уровне энергии орбитали s имеют самую низкую энергию. Максимальное количество электронов, которое может удерживать орбиталь, равно двум. Эти два электрона находятся в противоположном спине, так что отталкивание между двумя электронами сведено к минимуму.
орбитальный
Это орбитали в форме гантелей, энергия которых выше, чем у орбитали. Максимальное количество электронов, которое может удерживать орбиталь, равно 6. Это связано с тем, что одна орбиталь состоит из трех суборбиталей, называемых рИкс, пY и рZ, Каждая из этих орбиталей может содержать максимум 2 электрона.
орбитальный
Эти орбитали выглядят как две гантели в одной плоскости. Однако это более сложная трехмерная структура, чем s и p-орбитали. Одна орбиталь состоит из 5 суборбиталей. Каждая суборбиталь может содержать до 2 электронов. Следовательно, максимальное число электронов, которое может удерживать d-орбиталь, равно 10.

Рисунок 1: Формы атомных орбиталей
Согласно теории молекулярных орбиталей, когда две атомные орбитали перекрываются, образуется молекулярная орбиталь. Эта молекулярная орбиталь указывает на образование ковалентной связи. Поэтому орбитали непосредственно участвуют в химической связи.
Что такое уровни энергии
Электронные оболочки, которые расположены вокруг ядра, называются энергетическими уровнями. Эти оболочки имеют дискретные значения энергии. Электроны заполняют эти энергетические уровни или оболочки. Эти энергетические уровни называются K, L, M, N и т. Д. Энергетический уровень с самой низкой энергией - K. Электроны заполняются до этих энергетических уровней в соответствии с возрастающим порядком энергии. Другими словами, электроны сначала заполняются до самого низкого энергетического уровня. Таким образом, атомы могут стабилизироваться.
Есть фиксированные числа электронов, которые может удерживать каждый энергетический уровень. Эти цифры приведены ниже. Это число зависит от количества орбиталей, из которых состоит каждый энергетический уровень.
1 улица уровень энергии - 2
2 й уровень энергии - 8
3 й уровень энергии - 8
4 го уровень энергии - 8
Это указывает на то, что все другие уровни энергии, кроме 1 улица Уровень энергии может содержать до 8 электронов.

Рисунок 2: Уровни энергии в атоме. Символ «n» обозначает уровень энергии.
Электроны могут перемещаться между этими уровнями энергии, либо поглощая, либо выделяя энергию. Когда энергия передается атому, электрон с более низким энергетическим уровнем может быть перемещен на более высокий энергетический уровень. Это новое состояние называется возбужденным состоянием. Однако это возбужденное состояние не является стабильным. Следовательно, этот электрон может вернуться на уровень земли, высвободив энергию. Эти процессы называются электронными переходами.
Взаимосвязь между орбиталями и уровнями энергии
- Орбитали атома расположены в соответствии с их энергиями. Следовательно, уровни энергии состоят из орбиталей.
Разница между орбиталями и уровнями энергии
Определение
орбитали: Орбиталь - наиболее вероятная область, где электрон может быть найден вокруг ядра.
Уровни энергии: Энергетические уровни - это электронные оболочки, которые расположены вокруг ядра.
Именование
орбитали: Орбитали называются s, p, d и f.
Уровни энергии: Уровни энергии называются K, L, M, N.
Количество электронов
орбитали: Орбитали могут содержать максимальное количество электронов в соответствии с орбиталью, например, s = 2, p = 6 и d = 10.
Уровни энергии: Первый энергетический уровень состоит из 2 электронов, а все остальные энергетические уровни могут содержать до 8 электронов.
Заключение
Орбитали состоят из электронов. Уровни энергии показывают расположение орбиталей вокруг атома в соответствии с энергией этих орбиталей. Основное различие между орбиталями и энергетическими уровнями состоит в том, что орбитали показывают наиболее вероятный путь движения электрона, который движется вокруг ядра, тогда как энергетические уровни показывают относительное расположение орбиталей в соответствии с количеством энергии, которую они имеют.
Мы приступаем к изучению химии - мира молекул и атомов. В этой статье мы рассмотрим базисные понятия и разберемся с электронными формулами элементов.
Атом (греч. а - отриц. частица + tomos - отдел, греч. atomos - неделимый) - электронейтральная частица вещества микроскопических размеров и массы, состоящая из положительно заряженного ядра (протонов) и отрицательно заряженных электронов (электронные орбитали).
Описываемая модель атома называется "планетарной" и была предложена в 1913 году великими физиками: Нильсом Бором и Эрнестом Резерфордом

Протон (греч. protos - первый) - положительно заряженная (+1) элементарная частица, вместе с нейтронами образует ядра атомов элементов. Нейтрон (лат. neuter - ни тот, ни другой) - нейтральная (0) элементарная частица, присутствующая в ядрах всех химических элементов, кроме водорода.
Электрон (греч. elektron - янтарь) - стабильная элементарная частица с отрицательным электрическим зарядом (-1), заряд атома - порядковый номер в таблице Менделеева - равен числу электронов (и, соответственно, протонов).
Запомните, что в невозбужденном состоянии атом содержит одинаковое число электронов и протонов. Так у кальция (порядковый номер 20) в ядре находится 20 протонов, а вокруг ядра на электронных орбиталях 20 электронов.

Я еще раз подчеркну эту важную деталь. На данном этапе будет отлично, если вы запомните простое правило: порядковый номер элемента = числу электронов. Это наиболее важно для практического применения и изучения следующей темы.
Электронная конфигурация атома
Электроны атома находятся в непрерывном движении вокруг ядра. Энергия электронов отличается друг от друга, в соответствии с этим электроны занимают различные энергетические уровни.
Состоит из s-подуровня: одной "1s" ячейки, в которой помещаются 2 электрона (заполненный электронами - 1s 2 )
Состоит из s-подуровня: одной "s" ячейки (2s 2 ) и p-подуровня: трех "p" ячеек (2p 6 ), на которых помещается 6 электронов
Состоит из s-подуровня: одной "s" ячейки (3s 2 ), p-подуровня: трех "p" ячеек (3p 6 ) и d-подуровня: пяти "d" ячеек (3d 10 ), в которых помещается 10 электронов
Состоит из s-подуровня: одной "s" ячейки (4s 2 ), p-подуровня: трех "p" ячеек (4p 6 ), d-подуровня: пяти "d" ячеек (4d 10 ) и f-подуровня: семи "f" ячеек (4f 14 ), на которых помещается 14 электронов

Зная теорию об энергетических уровнях и порядковый номер элемента из таблицы Менделеева, вы должны расположить определенное число электронов, начиная от уровня с наименьшей энергией и заканчивая к уровнем с наибольшей. Чуть ниже вы увидите несколько примеров, а также узнаете об исключении, которое только подтверждает данные правила.
Подуровни: "s", "p" и "d", которые мы только что обсудили, имеют в определенную конфигурацию в пространстве. По этим подуровням, или атомным орбиталям, движутся электроны, создавая определенный "рисунок".
S-орбиталь похожа на сферу, p-орбиталь напоминает песочные часы, d-орбиталь - клеверный лист.

Правила заполнения электронных орбиталей и примеры
- Сперва следует заполнить орбитали с наименьшей энергией, и только после переходить к энергетически более высоким
- На орбитали (в одной "ячейке") не может располагаться более двух электронов
- Орбитали заполняются электронами так: сначала в каждую ячейку помещают по одному электрону, после чего орбитали дополняются еще одним электроном с противоположным направлением
- Порядок заполнения орбиталей: 1s → 2s → 2p → 3s → 3p → 4s → 3d → 4p → 5s → 4d → 5p → 6s
Должно быть, вы обратили внимание на некоторое несоответствие: после 3p подуровня следует переход к 4s, хотя логично было бы заполнить до конца 4s подуровень. Однако природа распорядилась иначе.
Запомните, что, только заполнив 4s подуровень двумя электронами, можно переходить к 3d подуровню.
Без практики теория мертва, так что приступает к тренировке. Нам нужно составить электронную конфигурацию атомов углерода и серы. Для начала определим их порядковый номер, который подскажет нам число их электронов. У углерода - 6, у серы - 16.
Теперь мы располагаем указанное количество электронов на энергетических уровнях, руководствуясь правилами заполнения.
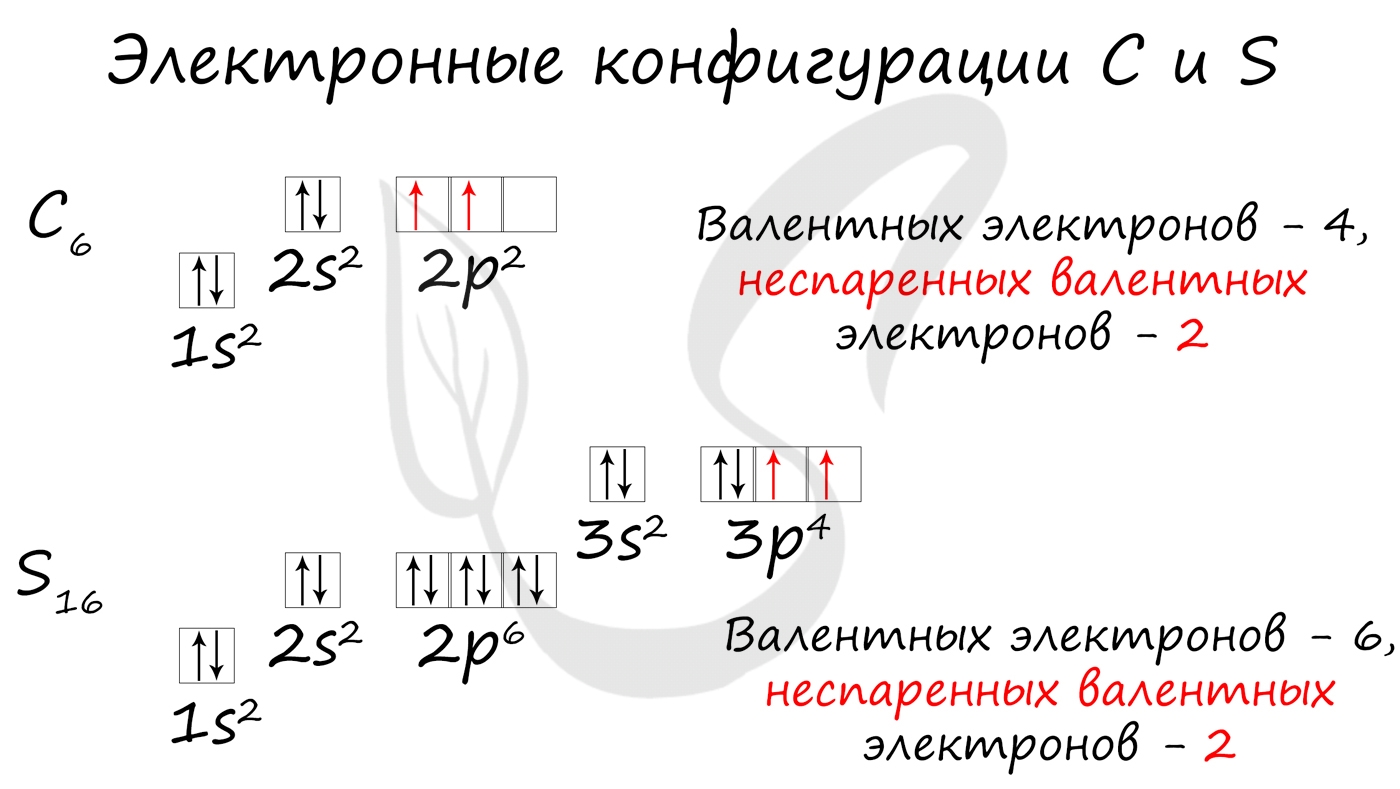
Обращаю ваше особе внимание: на 2p-подуровне углерода мы расположили 2 электрона в разные ячейки, следуя одному из правил. А на 3p-подуровне у серы электронов оказалось много, поэтому сначала мы расположили 3 электрона по отдельным ячейкам, а оставшимся одним электроном дополнили первую ячейку.
- Углерод - 1s 2 2s 2 2p 2
- Серы - 1s 2 2s 2 2p 6 3s 2 3p 4
Внешний уровень и валентные электроны
- Углерод - 2s 2 2p 2 (4 валентных электрона)
- Сера -3s 2 3p 4 (6 валентных электронов)
Неспаренные валентные электроны способны к образованию химической связи. Их число соответствует количеству связей, которые данный атом может образовать с другими атомами. Таким образом неспаренные валентные электроны тесно связаны с валентностью - способностью атомов образовывать определенное число химических связей.
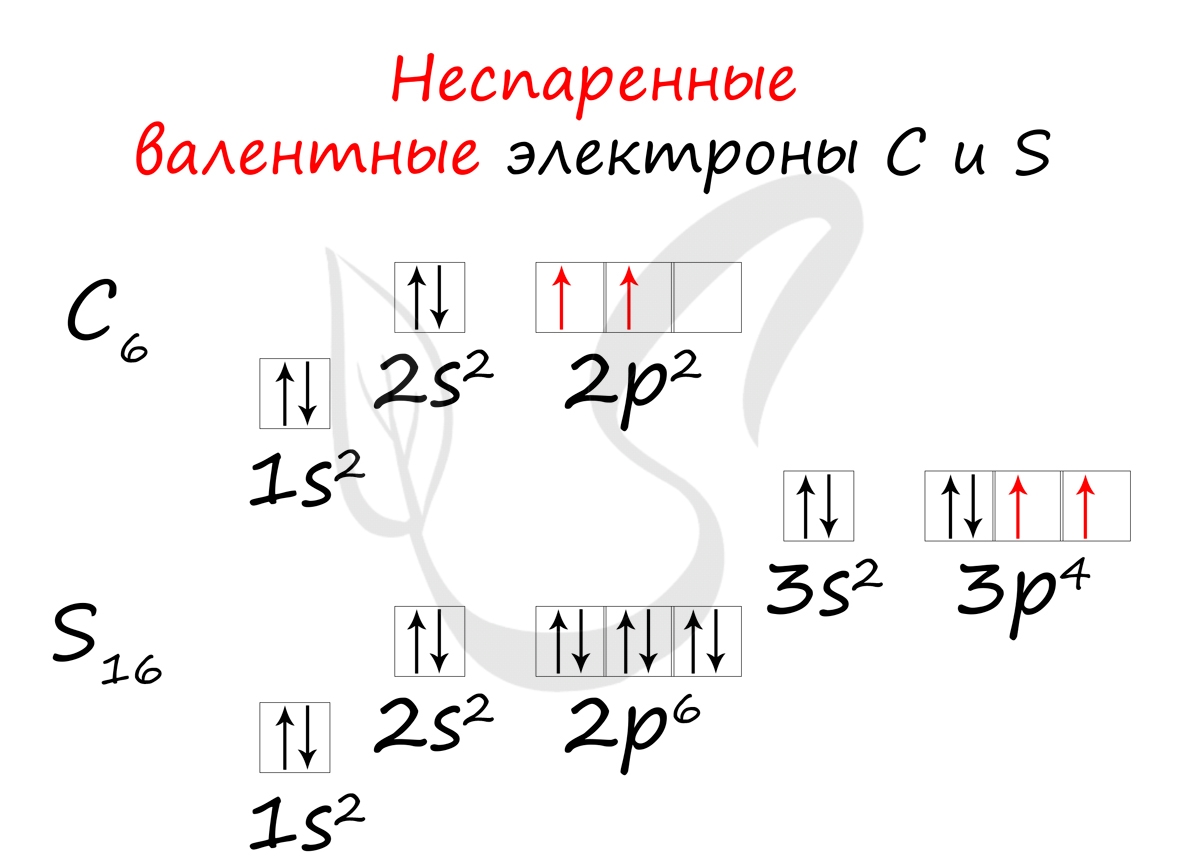
- Углерод - 2s 2 2p 2 (2 неспаренных валентных электрона)
- Сера -3s 2 3p 4 (2 неспаренных валентных электрона)
Тренировка
Потренируйтесь и сами составьте электронную конфигурацию для магния и скандия. Определите число электронов на внешнем (валентном) уровне и число неспаренных электронов. Ниже будет дано наглядное объяснение этой задаче.
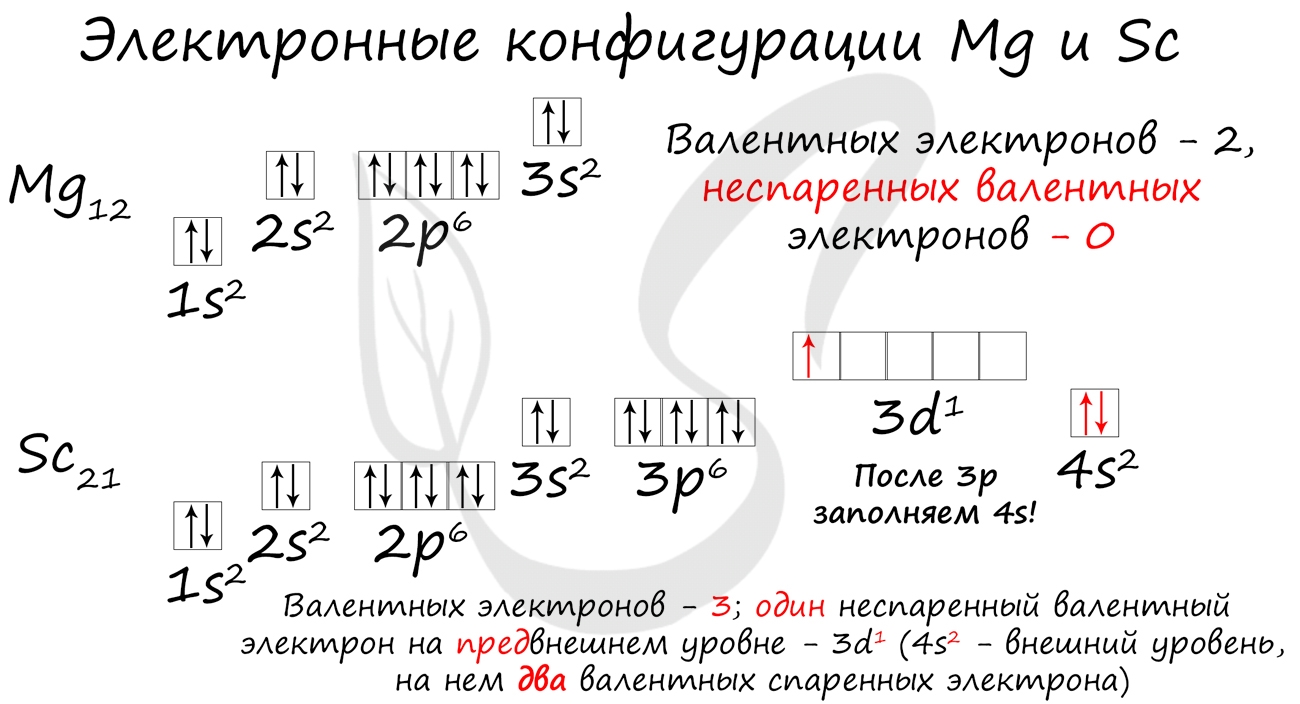
- Магний - 1s 2 2s 2 2p 6 3s 2
- Скандий - 1s 2 2s 2 2p 6 3s 2 3p 6 4s 2 3d 1
Читайте также:


